 2021 ASPEN 成人危重症患者的营养支持治疗
2021 ASPEN 成人危重症患者的营养支持治疗
# 2021 ASPEN 成人危重症患者的营养支持治疗
# 摘要
背景介绍 本指南更新了 2016 年美国肠外和肠内营养学会(ASPEN)/ 危重病医学会(SCCM)危重病营养指南中关于危重病营养支持的五个核心基础问题的建议。 方法 建议、评估、发展和评价的分级(GRADE)过程被用来发展和总结临床实践建议的证据。评估了以下临床结果:(1) 较高与较低的能量剂量;(2) 较高与较低的蛋白质剂量;(3) 纯等量肠外营养 (PN) 与肠内营养 (EN);(4) 补充 PN (SPN) 加 EN 与单独 EN;(5A) 脂肪乳复方制剂 (ILEs) 与大豆油;以及 (5B) 含鱼油 (FO) 的 ILE 与非 FO ILE。为了评估安全性,以体重为基础的能量摄入和蛋白质与医院的死亡率进行了对比。 结果 在 2001 年 1 月 1 日至 2020 年 7 月 15 日期间,确定了 2320 条引文,并从包括 20578 名参与者的 36 项试验中提取了数据。接受 FO 的患者的肺炎发生率下降,但临床意义不确定。除此之外,在任何问题上的任何结果都没有差异。由于缺乏关于危害的确定性,能量处方的建议被降低到 12-25 千卡 / 公斤 / 天。 结论 在众多的营养干预措施中,包括更高的能量或蛋白质摄入、等热量的 PN 或 EN、SPN 或不同的 ILE,没有发现临床结果的差异。随着更多一致的重症监护营养支持数据的出现,更精确的建议将成为可能。在此期间,需要临床判断和密切监测。本文经 ASPEN 董事会批准。
# 目的
大多数危重病人无法提供自己的营养。在这些病人中,经常提供人工营养。本指南的目的是总结营养支持方面的证据,以指导医生为危重病人提供人工营养,并对几个基础性问题提供 / 更新建议,这些问题是为大多数危重病人提供营养支持的核心。
现有的美国肠外和肠内营养学会(ASPEN)临床指南每 5 年或当文献中出现重大的新内容时(以先发生者为准),都会对其进行审查,以便进行更新。早期的指南为很少有随机对照试验(RCT)的大量临床决策提供了广泛的实践指导,产生了许多 "专家共识" 建议 1,而目前的指南将建议分级、评估、发展和评价(GRADE)过程限制在试验所探讨的问题上。这导致整体问题较少,一些建议并没有直接转化为营养支持处方。在本指南发布后,将有一份单独的临床建议文件来回答之前指南中的专家意见问题和其他没有充分证据的问题。为了帮助读者做出实践决策,在表 1 中每个 GRADE 问题下面都增加了 "临床应用" 一行,为如何将 GRADE 建议应用于实践提供指导。为了提高外部有效性和与当今重症监护室(ICU)患者的可比性,只包括 2001 年 1 月 1 日至 2020 年 7 月 15 日之间的 RCT,以反映现代更多的营养支持实践,此时的常规护理包括维持血糖控制,避免过度喂食能量,以及改善导管护理。特别重视试验中为患者提供的营养方面(即能量、蛋白质和脂肪乳剂 [ILE]),以及营养输送的时间和途径。
表 1. 指南问题、证据等级、建议摘要和临床应用
| 指南问题 | GRADE 证据等级 | GRADE 推荐意见 | GRADE推荐强度 |
|---|---|---|---|
| 1. 在成人危重病人中,能量摄入高低是否影响临床预后? | 中 | 在能量摄入水平较高与较低的患者之间,临床预后无明显差异。建议在ICU住院的前 7-10 天,以12-25 kcal/kg 的热卡进行喂养(取各研究的平均能量摄入范围)。 | 弱 |
| 关于问题1的临床应用的讨论:医生应该依靠临床判断。当EN或PN涉及血糖控制、呼吸性酸中毒或血清甘油三酯升高时,应考虑是否减少喂养的量。含有脂肪的镇静剂也会提供能量,应算入每日总摄入量中。胃肠道的耐受性会限制EN的量。 EN 喂养量达不到营养摄入的参考水平,可能会有维生素、矿物质和微量元素摄入不足的风险。 | |||
| 2. 在成人危重病人中,蛋白质摄入量高低是否会影响临床预后? | 低 | 有限证据表明,临床预后没有差异。由于高质量证据的试验太少,对2016年指南推荐的 1.2-2.0 g/(kg·d) ,目前无更新。 | 弱 |
| 3.在适合 EN 的成人危重病人中,在病重第一周,能量摄入相当时,主要喂养方式选择 PN 或 EN 是否会影响临床预后? | 高 | 在临床预后方面没有明显差异。因为能量摄入相当时,PN 并不优于 EN,且危害上无差异,故推荐为PN或EN皆可。 | 强 |
| 关于问题3的临床应用的讨论:本研究结果表明,当在危重病早期通过PN或EN提供的能量相当,且时间相对较短时,临床预后相似。鉴于这些证据,在危重病早期给予EN与PN的费用和便利性可能是决定喂养途径的更主要的因素,而非依据临床预后上的差异。当无法实施EN或EN不耐受时,或在有严重胃肠道疾病的患者中,就会面临使用PN的问题,这类患者不属于问题3的研究对象。两项试验报告的热卡为 18-20 kcal/(kg·d)、蛋白质为 0.6-0.8 g/(kg·d),并且 PN 都使用了预混配方。有关PN使用最重要的考量可能是在能量上避免过度喂养。最佳的血糖控制和导管护理也是 PN 使用中减少感染并发症的重要因素。临床判断个体患者对葡萄糖(监测血糖的控制)、脂肪乳(监测血清甘油三酯浓度)和氨基酸用量的代谢耐受性是实施恰当 PN 喂养的关键。 | |||
| 4. 在接受 EN 的成人危重病人中,在病重第一周给不给 SPN,是否会影响临床预后? | 高 | 临床预后无明显差异。基于在 ICU入 院早期提供 SPN 没有临床意义,推荐在ICU入院后前7天不启用 SPN。 | 强 |
| 关于问题4临床应用的讨论:本指南中的数据比较了ICU治疗第一周内的 SPN,并排除了营养不良的患者。这些研究结果意味着,一般的危重病人不会因为等待一周才开始 SPN 而有危害。此外,病人对EN的耐受性可能会在这个时间窗得以改善。然而,营养不良的病人或瘦肌肉较少的病人的需求并不在这些试验中,可能与营养正常的病人的需求不同。对于这些特殊情况,在头7天开始使用SPN时,应采用针对患者的临床判断。 | |||
| 指南问题5A. 在接受 PN 的成人危重病人中,提供复方制剂 ILE(即中链甘油三酯、橄榄油、FO、多种油),与100% 大豆油 ILE 相比,是否会影响临床预后? | 低 | 由于关键预后指标上统计学或临床上无显著差异,建议对适合启用 PN 的重症患者应用多种油 ILE 或 100% 大豆油ILE 皆可,包括在入住ICU后的第一周内。 | 弱 |
| 指南问题5B。在接受 PN 的成人重症患者中,使用的 ILE 含不含 FO,是否会影响临床预后? | 低 | 由于只有一项结果发现有显著差异,而且其他关键的下游指标没有数据支持,建议对适合启用 PN 的重症患者应用含或不含 FO 的 ILE 皆可,包括在入住ICU后的第一周内。 | 弱 |
| 关于临床应用问题5A和5B的讨论:除了 100% 的大豆油 ILE 外,美国现在还有含多种油和 FO 的 ILE 产品,但医疗机构这些配方的供应可能有所不同。一般来说,ILE 是一种安全和有效的能量来源,可以在开始使用 PN 配方时,包括在入住 ICU 后的第一周内,与 PN 配方一起使用。优化 ILE 的使用有助于避免过多使用葡萄糖和高血糖症。监测血清甘油三酯的浓度将提供有关脂质清除是否充分的信息。在对脂质和能量摄入的总体估计中,应考虑含有脂肪的镇静方案所提供的能量。如果 PN 需要超过10天,给予足够水平的必需脂肪酸以满足需求也很重要。多种油ILE 和含 FO 的 ILE 的必需脂肪酸含量低于大豆油 ILE。 | |||
缩略语。EN,肠内营养;FO,鱼油;GRADE,建议、评估、发展和评价的分级;ICU,重症监护室;ILE,脂质注射乳剂;PN,肠外营养;SPN,补充 PN。
# 指南的局限性
这些 ASPEN 临床指南是基于一组卫生专业人员的普遍共识,在制定这些指南时,他们研究了营养实践的好处和这种治疗的固有风险。ASPEN 召集了一个由临床流行病学 / 方法学专家、营养师、药剂师和医生组成的临床营养多学科专家工作组。这些人参与了指南的制定并共同撰写了本文件。本指南中的任何建议都不构成医疗或其他专业建议,不应视为医疗或其他专业建议。如果此处公布的信息可用于协助护理病人,这完全是主治医护人员的专业判断结果,其判断是优质医疗服务的主要组成部分。这里提供的信息不能代替医护人员的这种判断。在临床环境和患者适应症的情况下,可能需要采取与本文建议不同的行动,在这些情况下,应以治疗专家的判断为准。本文经 ASPEN 董事会批准。
该指南提供的建议得到了对现有文献的回顾和分析,以及专家意见和临床实用性的融合。目前的文献有其局限性,包括研究设计的差异性;对能量、蛋白质和 ILE 实际摄入水平的描述有限;患者样本和治疗策略的异质性;以及营养状况的信息有限和盲法的困难。由于大多数危重病人的电解质和液体不稳定,以及对喂养类型或细节(肠内营养 [EN] 与肠外营养 [PN]、蛋白质补充剂、输液泵速度等)的盲法不切实际,大多数研究对订购过程或管理喂养的护士或喂养内容的细节不设盲。
# 目标人群
目标人群是外科或内科重症监护室中无法维持自愿口服并由 PN 或 EN 支持的重症成人患者。
# 纳入标准
纳入的标准是 16 岁以上患者的 RCT,干预措施包括 EN 或 PN,报告临床上重要的结果(死亡率、ICU 或住院时间 [LOS]、生活质量或并发症),并以英语发表。
# 排除标准
排除了只包括生化、氮平衡、代谢、微生物或营养结果的研究;包括准随机化的研究;或只招募 16 岁或以下患者的研究。
# 目标受众
本指南供临床医生使用,包括但不限于营养师、护士、执业护士、药剂师、医生和 / 或为成年危重病人提供营养护理的医生助理;对危重病感兴趣的营养研究人员;以及负责评估营养支持政策的医院委员会。
# 定义
营养支持是指通过肠道接入设备提供的 EN 和 / 或静脉提供的 PN。危重病人也可能接受静脉输液或镇静药物,其中一些药物提供能量。
# 方法
专家工作组确定了文献检索所使用的关键词,制定了涉及当代主要实践主题的关键 PICO 问题,并确定了文献检索的时间框架、目标人群和要处理的具体结果。这些 PICO 问题确定了文献搜索的范围。我们计划在 5 年内或在有重要证据时重新审视本指南。
# 文献搜索
所有的引文都是从 PubMed/MEDLINE 数据库中筛选出来的,仅限于 2001 年 1 月 1 日至 2020 年 7 月 15 日之间发布的引文。搜索条件包括在图 1 中。我们的搜索策略旨在收集以下情况下的引文:(1)它们被 MEDLINE 索引,并且至少包含 1a 组和 1b 组的一个术语;(2)它们被 MEDLINE 索引,并且在引文标题或摘要中至少包含 2a 组和 2b 组的一个术语;或(3)它们被 PubMed 非 MEDLINE 数据库索引,并且至少包含 2a 组和 2b 组的一个术语。然后,搜索策略被进一步限制为只搜索那些与第 3 组所列术语交叉引用的引文。在 Embase 和 Cochrane Central 数据库中也采用了类似的搜索策略。

文献检索词。 lang,语言;MeSH,医学主题词;ptyp,出版物类型。
# 数据获取
每份摘要由两位作者独立筛选,以确定该研究是否符合纳入标准。使用标准化的数据摘要表(DAF)对符合所有三项纳入标准的文章进行审查,该表是根据指南的具体问题,使用 RCTs 的 GRADE 方法制定的。数据检索包括人口信息、用于评估能量和蛋白质需求的方法、接受的能量和蛋白质的数量(即暴露变量)、各种临床结果变量以及对调查质量的评估。有准随机化的试验被排除在外。每篇文章由两名工作组成员独立审查,比较结果,通过共识解决分歧,并为每项试验建立最终的 DAF。为了分析和比较研究结果的一致性,对于问题 1-4,"干预" 组被指定为那些随机接受更多和 / 或更早能量和 / 或更高蛋白质摄入的人;"对照" 组被定义为随机接受更少能量或蛋白质或延迟喂食的病人。对于问题 5A 和 5B,干预组被定义为提供多种油 ILE 或鱼油(FO)ILE 与豆油(SO)ILE 的患者。
# 证据质量评估
在评估 GRADE 方法中的证据质量时,要考虑五个主要因素。偏倚风险指的是研究设计(准随机化、缺乏盲法、基线时各组缺乏可比性)或执行(缺乏意向性治疗 [ITT] 分析、暴露不充分、随访损失过多)中的局限性。Cochrane 偏倚风险 2 工具(RoB2)3 被用来评估偏倚。需要注意的是,在这个新工具的背景下,偏倚不是对研究本身的评论,而是对研究回答我们每个单独结果的具体问题的能力的评论(即一项研究可能对一个结果有高的偏倚风险,对另一个结果有低的偏倚风险,这取决于所问的问题和研究的设计)。不一致是指在得出建议的各项试验中,结果存在大量无法解释的异质性。这是通过检查研究结果的一致性来评估的。间接性是一个主观术语,指的是现有证据对指南问题的直接适用程度。这是通过检查我们将研究结果应用于我们的人群和感兴趣的问题的能力的限制来评估的。不精确性是指我们对估计的效应大小反映真实效应大小的信心程度。这可以通过检查 CI 的宽度和评估检测效应的能力来评估。发表偏倚反映了研究结果的性质决定了其发表状态的可能性,从而使综合研究结果偏离文献中被遗漏的研究结果的方向。
GRADE 过程将证据体的质量评估与建议陈述的强度明确分开。这种分离使得采纳建议所带来的风险与收益的权重得以纳入。因此,尽管公布的证据相对较弱,但如果采用该建议的净收益超过了危害,那么该建议就可能是 "强" 的。另外,结合所纳入的试验的森林图可能会显示有统计学意义的差异(P≤0.05),但不是有临床意义的差异,无法支持强有力的建议。表 2 描述了分配给一项建议的 GRADE 的标准语言和理由。值得注意的是,为每个问题制定的临床应用并不是 GRADE 过程的一部分 -- 也就是说,它们并不代表 GRADE 数据的 "专家共识"。相反,它们是为了帮助医生在临床上应用我们的研究结果,而这些研究结果并没有直接转化为营养支持处方。
表 2. 指南建议的语言 a
| 证据的质量 | 权衡风险与效益 | 建议的强度 | 指南建议的语言 |
|---|---|---|---|
| 非常低至高 | 净收益大于危害 | 强烈建议 | 我们建议 |
| 非常低至高 | 净危害相当大,可能超过收益 | 弱 | 我们建议 |
- 注:在极少数情况下,临床小组可能决定不做推荐,但在几乎所有情况下,建议、评估、发展和评价的分级(GRADE)过程鼓励小组做出推荐,而不管证据如何。只要有可能,这些建议都是基于证据的。当这不可能时,它们被视为专家意见,这不是 GRADE 的一个类别。
# 统计分析
使用随机效应模型和 0.05 的 α 显著性水平对有三个或更多具有可比性数据的研究结果进行元分析。符合纳入标准的试验,其数据与问题相关,但相对于其他纳入的试验,其表现方式不同,在文中讨论,但不进行荟萃分析。计算干预组和对照组在结果变量方面的风险差异(RD)。RD 提供了关于干预组与对照组相比,暴露对临床结果风险的绝对影响的信息。任何一组的风险都是通过事件的数量除以事件风险的患者数量而得出。RD 是用干预组的事件风险直接减去对照组的事件发生风险。当干预组和对照组之间没有差异时,RD=0。RD 的 95% CI 包含 0,表明组间差异没有统计学意义。
RD 的这种影响和临床意义因发生事件的基本风险而改变,因此低风险事件的 RD 可能比基本风险较高的事件的相同 RD 更具临床意义。例如,如果对照组的风险是 0.02(2%),而干预组的风险是 0.04(4%),则干预措施使风险翻倍(RD=0.02)。相反,如果对照组的风险是 0.75(75%),干预组的风险是 0.77(77%),临床风险几乎没有增加,但 RD 是一样的(RD=0.02)。由于这个原因,在解释一个显著的 RD 时,考虑潜在的风险总是很重要的。
当试验数据不能合并估计效应大小时,在作者介绍数据时,在每个问题的汇总表中报告。所有的统计分析都在 Stata 16(StataCorp; College Station, TX)中进行。使用随机效应模型计算汇总统计数据并构建森林图。通过漏斗图和 Egger 统计数据评估出版偏倚,但只对至少有 10 项研究的主要文件森林图进行了评估(见支持性附录)。GRADEPRO 指南开发工具(Cochrane 合作组织,2020 年)被用来估计每个问题中每个结果的证据体的强度,并创建汇总表。然后用它来推断证据的总体质量,相对于它回答各自 PICO 问题的能力。
# 安全性分析
对于问题 1 和 2,为了便于推荐能量和蛋白质供应的具体切点,进行了事后安全分析(见支持性附录),目的是在每公斤能量的现有范围内定性评估医院死亡率。每项研究的随机分组被分开,并按每公斤能量的 X 轴排序。然后将其与医院死亡率作对比,并对线性趋势线进行定性评估。研究仅限于符合我们纳入标准的 RCTs,以及提供每公斤能量接收信息的研究。通过分层处理研究之间的进一步差异,如国家和医疗系统,以及研究是否包括所有进入 ICU 的病人和一个亚组,。我们还研究了按急性生理和慢性健康评估(APACHE)II 和身体质量指数(BMI)的中位数分层。额外的森林图被运行,以探索在其研究设计中使用不同干预措施(较高与较低的能量暴露,EN 与 PN,补充 PN [SPN] 与标准治疗)的能量暴露试验相结合。此外,还研究了以低热量干预或强化营养干预为目的的研究分层,以及按每公斤所接受的能量的组间分离排序和分层的森林图。
# 结果
我们的搜索策略发现了 2320 篇引文。其中,138 篇引文被下载用于进一步评估。经过审查,有 80 篇文章符合数据摘要的纳入标准,其中 36 项试验包含可用于回答所提出的问题的数据,因此,DAF 已经完成。
# 问题 1. 在成人危重病人中,提供较高与较低的能量摄入是否影响临床结果?
建议。在能量摄入水平较高与较低的患者之间,没有发现临床结果的明显差异。我们建议在 ICU 住院的前 7-10 天,喂食 12-25 千卡 / 公斤(即所考察的平均能量摄入量范围)。
证据的质量。中等
建议的强度。较弱
理由:这个广泛的建议反映了我们的森林图的两个主要组成部分,限制了它们的解释。首先,无法生成一个更具体的能量目标切点,因为这需要在不同的每公斤能量水平上对结果进行检查。不幸的是,这是不可能的,因为试验的能量暴露(表 3)之间存在重叠,而且干预和控制之间的研究内能量差异有限。第二,森林图分析假定感兴趣的暴露(即能量摄入)和结果之间存在线性关系;然而,能量 / 结果关系并没有被证明是线性的。为了解决这些局限性,我们进行了安全分析(见支持性附录),以直观地检查我们的数据是否有益处或危害的证据(图 S1-S59)。我们的广泛建议反映了我们数据中的平均能量暴露范围和安全分析的结果。这一决定是基于没有证据表明能量提供的益处,也缺乏确定性,这与过去指南建议中的建议一致。
表 3. 问题 1 的数据摘要:在成人危重病人中,提供较高与较低的能量摄入是否影响临床结果?
| 第一作者,年份 | 人口 | 高能量与低能量的比较 (n) | 提供的摄入量 | 感染,n (%) | 机械通气时间,中位数(IQR)或平均 ±SD,天数 | 住院时间,中位数(IQR)或平均 ±SD,天数 | 死亡率,n (%) |
|---|---|---|---|---|---|---|---|
| Arabi, 20115 | 成人内科 / 外科 ICU 患者平均 BMI:28.5 vs 28.5 | 90%-100% 目标能量(n = 120) vs 60%-70% 目标能量(n = 120) | 能量(千卡 / 天):1252±433 vs 1067±306 蛋白质(克 / 天):48±21 vs 44±19 | 败血症:56(47) vs 53(44) | 13.2 ± 15.2 vs 10.6 ± 7.6 | 重症监护室。14.5 ± 15.5 vs 11.7 ± 8.1 医院:67.2 ± 93.6 vs 70.2 ± 106.9 | 28 天:28(23)对 22(18)。ICU:26 (22) vs 21 (18) 医院:51 (43) vs 36 (30) 6 个月。52 (44) vs 38 (33) |
| Arabi,2014 年 4 | 成人内科 / 外科 ICU 病人平均 BMI:29.7 vs 29 | 70%-100% 目标(n = 446) vs 40%-60% 目标(n = 448) | 能量(千卡 / 天):1299 ± 467 vs 835 ± 297 蛋白质(克 / 天):59±25 vs 57±24 | 肺炎:90 (20) vs 81 (18) 任何感染。169 (38) vs 161 (36) | 10(5-16) vs 9(5-15) | 重症监护室。13 (8-20) vs 13 (8-21) 医院。30 (14-63) vs 28 (15-54) | 28 天:97 (22) vs 93 (21) ICU:85(19)对 72(16)。医院:123(28)对 108(24)。90 天:127(29)对 121(27)。180 天:140(32)对 131(30)。 |
| 布伦瑞克,2015 年 5 | 内科 ICU 的 ALI 患者 BMI≥30,45% vs 47 | 强化治疗 b(n = 40) vs 标准治疗(n = 38) | 能量(千卡 / 公斤 / 天):25.4 ± 6.6 vs 16.6 ± 5.6 蛋白质(克 / 天):82±23 vs 60.4±24 | 任何感染。5 (12) vs 8 (21) | 6(4-10) vs 7(3-14) | ICU。15.5 ± 12.8 vs 16.1 ± 11.5 医院:27.2±18.2 vs 22.8±14.3 | 死亡率:16(40) vs 6(16) |
| Chapman, 201812 | 46 个 ICU 中机械通气并符合 EN 条件的成人患者平均 BMI:29.2 vs 29.3 | 1.5 千卡 / 毫升(n = 1971) vs 1.0 千卡 / 毫升(n = 1986)配方按每公斤 IBW 1 毫升给药 | 基于 IBW 的能量(千卡 / 公斤 / 天):30.2±7.5 vs 21.9±5.6 基于 ABW 的能量(千卡 / 公斤 / 天):23.9(7.8) vs 17.4(5.5)。 | 菌血症:228(12) vs 221(11) | NR | NR | 医院。468 (24) vs 470 (24) 28 天:450 (23) vs 455 (23) 90 天:523(27)对 505(26)。 |
| Charles,2014 年 4 | 外科 ICU 的成人患者平均 BMI:28.1 vs 32.9 | 标准 25-30 千卡 / 公斤(n = 42) vs 12-15 千卡 / 公斤(n = 41) | 能量(千卡 / 公斤 / 天):17.1 ± 1.1 vs 12.3 ± 0.7 蛋白质(克 / 公斤 / 天):1.1 ± 0.1 vs 1.1 ± 0.1 | 菌血症:8 (19) vs 10 (24) 肺炎:20 (48) vs 18 (44) 任何感染。32 (76) vs 29 (71) | NR | ICU:c13.5 ± 1.1 vs 16.7 ± 2.7 医院:C31±2.5 vs 35.2±4.9 | 死亡率:4(10) vs 3(7) |
| Desachy, 2008 年 8 | 机械通气的病人平均 BMI:25 vs 27 | 立即入院(n = 50) vs 逐步入院(n = 50) | 能量(千卡 / 天):1715 ± 331 vs 1297 ± 331 蛋白质(克 / 天):82±23 vs 60.4±24 | 肺炎:0 (0) vs 0 (0) | NR | 重症监护室。15 ± 11 vs 15 ± 11 医院:56±59 vs 51±75 | ICU: 6 (12) vs 8 (16) 医院:14 (28) vs 11 (22) |
| Doig, 201317 | 31 个内 / 外科 ICU 中短期内禁忌使用 EN 的重症患者平均 BMI:27.9 vs 28.5 | 早期 PN(n = 681)与标准治疗(n = 682)(两组都接受 EN)。 | 能量(千卡 / 公斤 / 天)。NR 蛋白质。NR | 肺炎:43 (6) vs 45 (7) 菌血症:39 (6) vs 33 (5) 任何感染。74 (11) vs 78 (11) | NR | ICU:a8.6(8.2-9) vs 9.3(8.9-9.7) 医院:A25.4 (24.4-26.6) vs 24.7 (23.7-25.8) | ICU:81 (12) vs 100 (15) 医院:140 (21) vs 151 (22) 60 天:146 (22) vs 155 (23) |
| Doig, 20159 | 13 个内 / 外科 ICU 的患者平均 BMI:28 vs 28 | 标准治疗(n = 165) vs 2 天,每小时 20 千卡,然后逐渐增加到平时(n = 166)。 | 能量(千卡 / 公斤 / 天)。NR 蛋白质。NR | 肺炎:22 (13) vs 14 (8) 菌血症:8(5)对 2(1)。任何感染:27 (16) vs 13 (8) | A7.45 (7.16 to 7.65) vs 7.86 (7.54 to 8.18) | ICU:A10.0(9.2-10.9) vs 11.4(10.5-12.4)。医院:A21.7 (20.0-23.5) vs 27.9 (25.7-30.3) | 重症监护室。15 (9) vs 9 (5) 医院: 30 (18) vs 15 (9) 60 天:35 (21) vs 15 (9) 90 天:35 (21) vs 21 (13) |
| Peake, 201410 | 外科 ICU 的成人危重病人平均 BMI:27.8 vs 26.2 | 1.5 千卡 / 毫升(n = 57) vs 1.0 千卡 / 毫升(n = 55) | 能量(千卡 / 公斤 / 天):27.3±7.4 vs 19.0±6.0 蛋白质(克 / 公斤 / 天):1.0 ± 0.3 vs 1.1 ± 0.3 | NR | NR | ICU:9.6(5.9-22.6) vs 11.8(6.9-22.8)医院。34.5 (16.9-83.6) vs 30.6 (15.2 - 未定义) | ICU:6 (11) vs 9 (16) 医院:10 (19) vs 14 (27) 28 天:11 (20) vs 18 (33) 90 天:11 (20) vs 20 (37) |
| Petros, 201611 | 内科重症监护室的成人患者平均 BMI:27.1 vs 28.6 | 正常热量(n = 54) vs 低热量(n = 46)EN 或 PN | 能量(千卡 / 公斤 / 天):19.7 ± 5.7 vs 11.3 ± 3.1 蛋白质(克 / 公斤 / 天)。NR | 任何感染。6 (11) vs 12 (26) | 7.44 (2.90-16.80) vs 10.60 (4.81-28.60) | NR | ICU。12 (22) vs 10 (22) 医院:17 (32) vs 17 (37) 28 天:18 (33) vs 18 (39) |
| 赖斯,2011 年 14 | 内科重症监护室的呼吸衰竭成人患者平均 BMI:28.2 vs 29.2 | 正常热量(n = 102) vs 营养性 EN(n = 98) | 能量(千卡 / 天):1418±686 vs 300±149 蛋白质(克 / 天):54.4 ± 33.2 vs 10.9 ± 6.8 | 肺炎:18(18) vs 14(14)任何感染。33 (32) vs 30 (31) | NR | 无 ICU 天数:21 (9.3-24) vs 21 (6.5-24) 无住院天数。16.5 (0-21) vs 12 (0-21) | 医院:20 (20) 正常饮食 vs 22 (22) 营养性饮食 |
| Rice, 201213 | 44 个 ICU 的成人 ALI 患者平均 BMI:30.4 vs 29.9 | 25-30 千卡 / 公斤的全 EN 喂养(n = 492) vs 营养型(n = 508)。 | NR | 菌血症:46(9) vs 59(12) 肺炎:33 (7) vs 37 (7) | NR | 28 天内无 ICU 天数:a 14.7 (13.8-15.6) vs 14.4 (13.5-15.3) | 60 天:109 (22) vs 118 (23) |
| Rugeles,2016 年 16 | 内 / 外科 ICU 中预计需要 EN>96 小时的成人患者平均 BMI:25 vs 25 | 正常热量(n = 60) vs 低热量(n = 60) | 能量(千卡 / 公斤 / 天):a 19.2 ± 4.3 vs 12.1 ± 2.6 蛋白质(克 / 公斤 / 天):a1.3 ± 0.3 vs 1.3 ± 0.3 | NR | 9(8.3) vs 9(8.3) | ICU。10.5(8.0) vs 12(7.3) | 28 天:16 (27) vs 18 (30) |
| Singer, 2011115 | 成人内科 / 外科 ICU 平均 BMI:27.8 vs 27.4 | 间接量热法 - 测量需求(n = 65) vs 25 kcal/kg/day(n = 65) | 能量(千卡 / 天):2086 ± 460 vs 1480 ± 356 蛋白质(克 / 天):76±16 vs 53±16 | 菌血症:13 (20) vs 8 (12.3) 肺炎:18 (27.7) vs 9 (13.8) | 16.1±14.7 vs 10.5±8.3 | ICU。17.2±14.6 vs 11.7±8.4 医院。33.8 ± 22.9 vs 31.8 ± 27.3 | 重症监护室。16 (25) vs 17 (26) 医院:21 (32) vs 31 (48) |
- 缩略语。ABW,实际体重;ALI,急性肺损伤;BMI,体重指数(kg/m2);EN,肠内营养;IBW,理想体重;ICU,重症监护室;IQR,四分位数范围;Med,医疗;NR,未报告;PN,肠外营养;手术,手术。
要纳入这个问题的分析,试验需要在不引起次要竞争性干预(如从 EN 转向 PN)的情况下随机化能量暴露。虽然这个问题是关于任何来源的一般能量摄入的更广泛的问题,但作为敏感性分析,蛋白质剂量也被认为是一个潜在的竞争性干预。因此,下面的森林图既包含了综合结果,也包含了按试验是否为等氮分配组分层的结果。13 项试验 4-16 代表 8690 名患者的数据被纳入回答这个问题(表 3)。由于认识到问题 3 中报告的 PN 和 EN 之间缺乏差异,安全分析还包括一系列图,在其分析中结合了问题 1、3 和 4 的这些研究。
各项试验的方法学质量和干预设计各不相同。一项试验 11 报告了重要的基线差异,包括基线糖尿病患病率的不平衡,这些差异在他们的分析中没有得到控制。两项试验 9, 17 缺乏真正的 ITT 设计,在参与者撤回同意后将其从分析中删除。由于退出人数较少,且不可能影响结果,因此将其纳入本分析中。大多数试验包括所有进入 ICU 的病人,4-6,9-11,14,15,17,但有些试验将入选范围限制在急性呼吸窘迫综合症(ARDS)7,13 或需要机械通风的病人。能量的提供被报告为每天每公斤的千卡路里 7,10-12,16 或每天的平均或中位千卡路里,4,5,8,14,15,三项试验没有包括提供能量或蛋白质摄入的数据。14, 17 在报告每公斤热量的试验中,高喂养组的摄入量从 17 到 30 千卡 / 公斤不等。6, 10 在报告数据为平均值或中位数的试验中,较高的摄入量从 1252 到 2085 千卡 / 天不等。此外,高能量组和低能量组之间提供的能量差异很大(从 Charles 等人 6 的研究中的 5 千卡 / 千克 / 天到 Braunschweig 等人 7 的研究中的 9 千卡 / 千克 / 天,从 Arabi 等人 5 的研究中的 200 千卡到 Rice 等人 14 的研究中的 1100 千卡 / 天,分别)。对于没有提供每天每公斤千卡能量测量值或分别提供千卡和公斤测量值的研究,为防止其标准误差的混淆,提供了每天千卡的能量测量。如前所述,尽管将试验分为较高与较低的能量摄入是必要的,以允许在所有纳入的试验中进行森林图的比较,但它假定能量暴露(以每公斤千卡热量测量)的影响与结果有线性关系,这与以前的研究结果相冲突。此外,这些森林图并不能确定数据的切点或拐点。为此,我们必须研究每公斤能量的不同水平的关系,而研究的能量暴露之间的重叠使我们不可能在森林图中做到这一点。 由于上述的间接性问题,证据的质量被评为中等。这是基于我们的关键结果,即医院死亡率。我们的建议强度被评为弱,因为我们对危害和益处缺乏确定性。
在任何临床结果方面,高能量摄入组与低能量摄入组之间没有发现明显的差异。研究较高与较低能量摄入之间关系的试验有不同的发现,一些试验支持较高的能量输送水平的好处,9,11 其他试验表明有危害,5,7,15 而大多数试验发现组间没有明显的差异。六项试验 4-6,10,12,16 提供了等氮的能量,但没有影响能量暴露对我们选择的任何结果的影响(图 2-11)。综合来看,目前的证据表明,较高的能量暴露(这里报告的最高值是 30 千卡 / 公斤 / 天 12)和较低的能量暴露(这里报告的最低值是 300 千卡 / 天 14)对危重病人的结果影响(或没有影响)是相似的。在能量摄入较高与较低的患者中,菌血症的风险没有区别(RD=0.01;95% CI,-0.02 至 0.03;P=0.58)(图 2)。无论是等氮还是非等氮试验,都没有显示出较高和较低能量摄入之间的菌血症风险的显著差异。
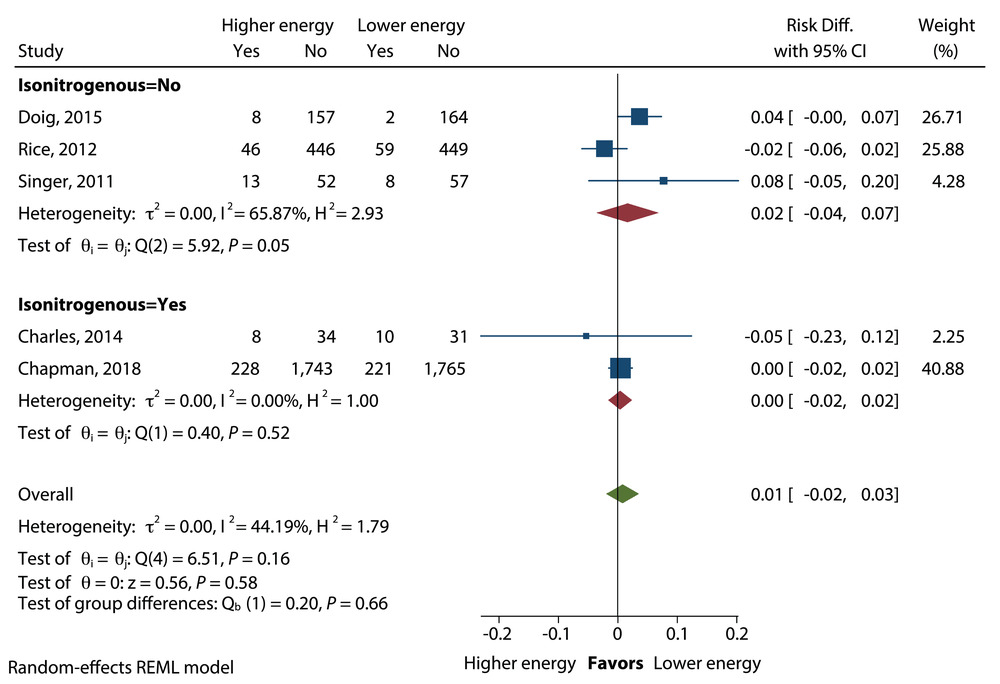
能量摄入量较高与较低的患者在菌血症方面的平均差异。差异,差异;REML,限制性最大似然。
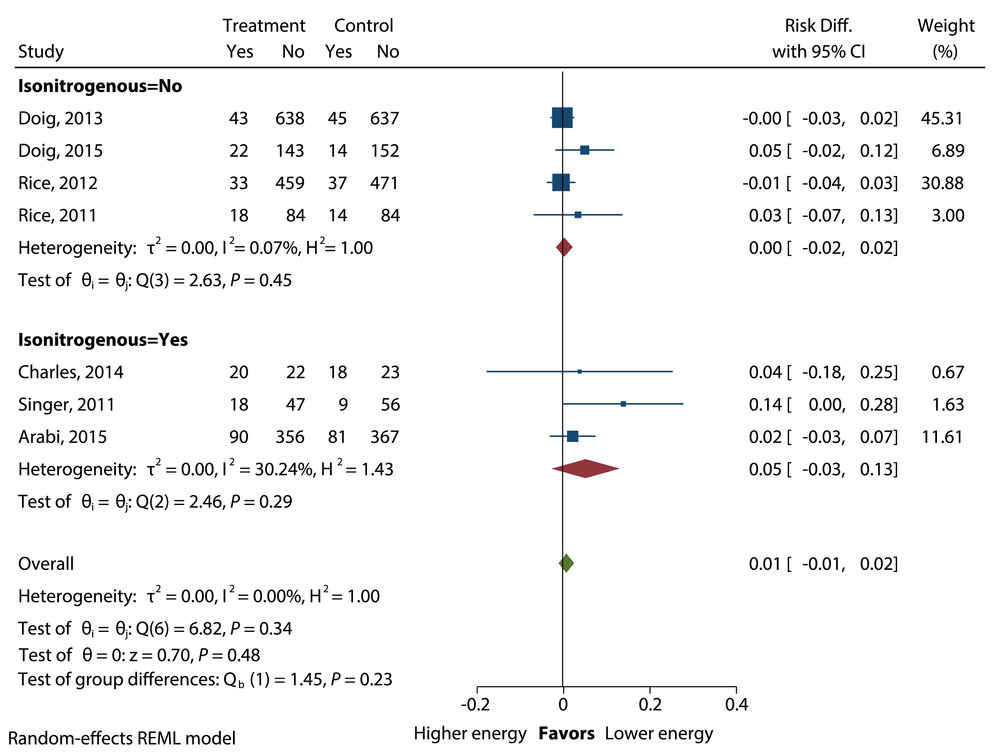
高能量摄入与低能量摄入患者的肺炎的平均差异。差异,差异;REML,限制性最大似然。
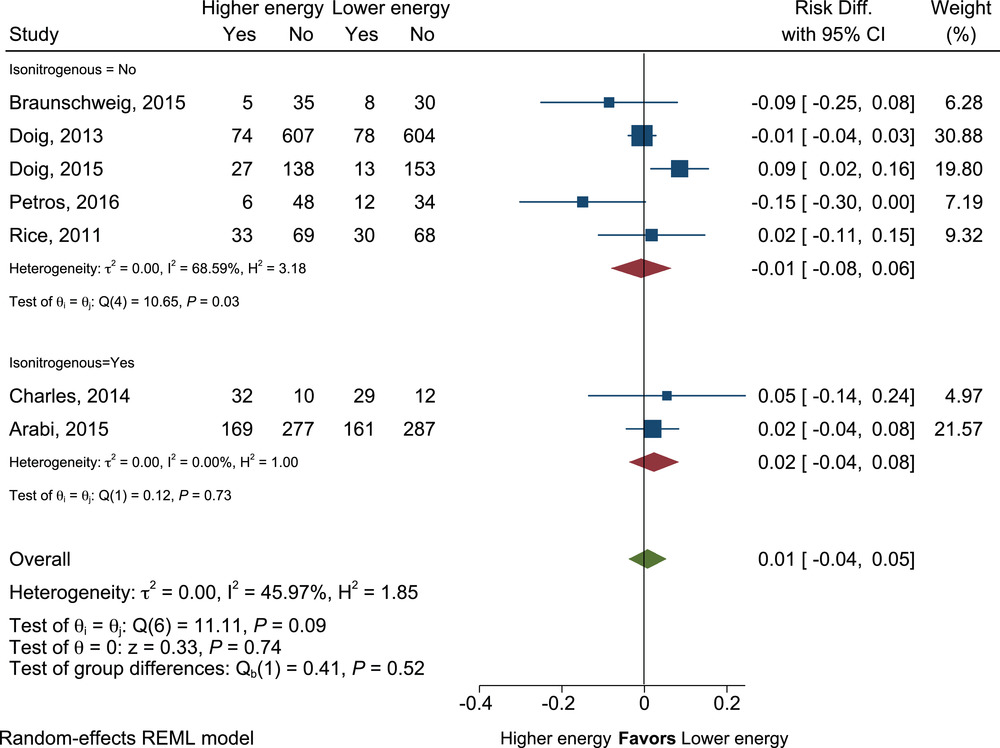
能量摄入较高与较低的患者任何感染的平均差异。Diff.,差异;REML,限制性最大似然。
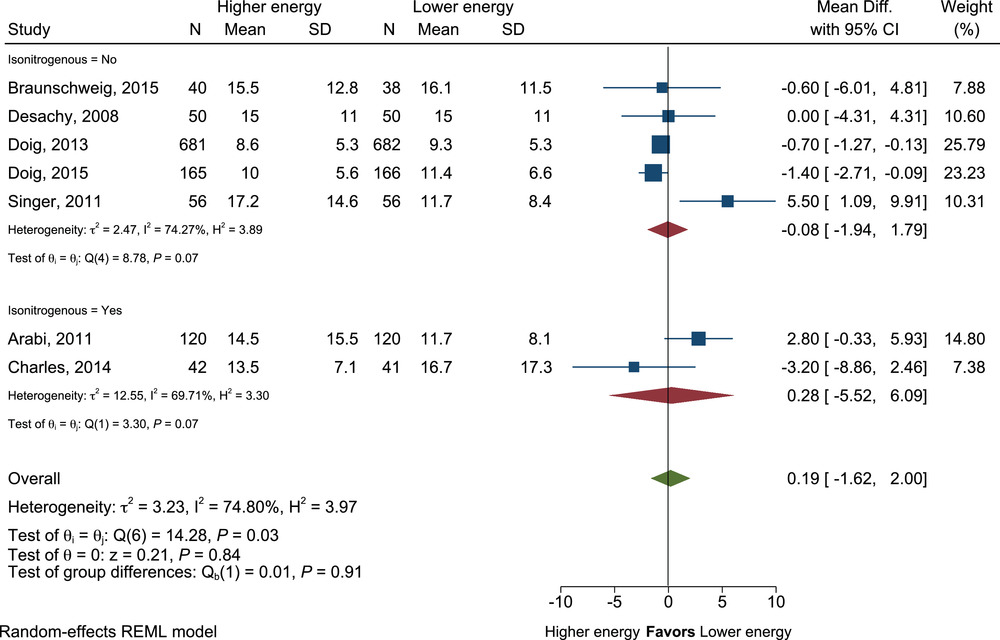
能量摄入较高与较低的患者在重症监护室停留时间的平均差异。差异,差异;REML,限制性最大似然。
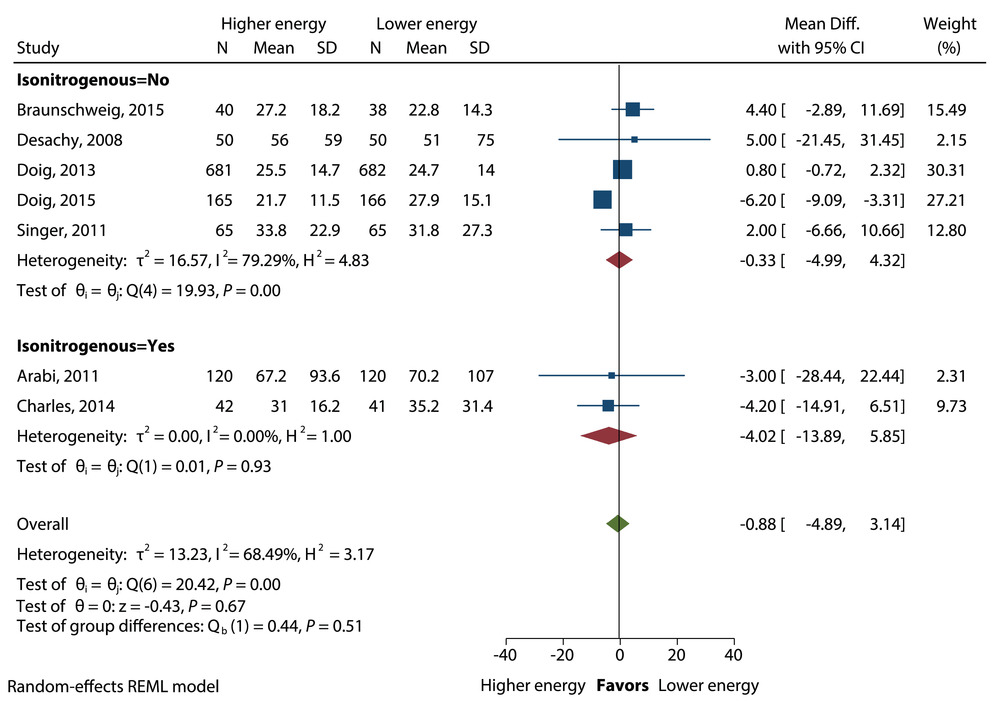
能量摄入较高与较低的患者住院时间的平均差异。差异,差异;REML,限制性最大似然。
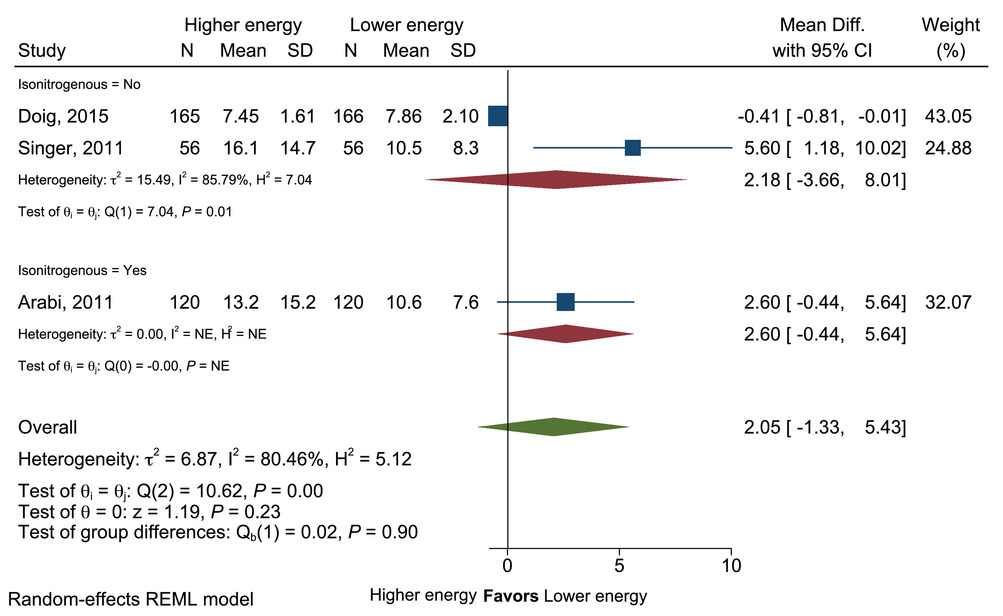
能量摄入量较高与较低的患者呼吸机天数的平均差异。Diff.,差异;NE,不可估计;REML,限制性最大似然。
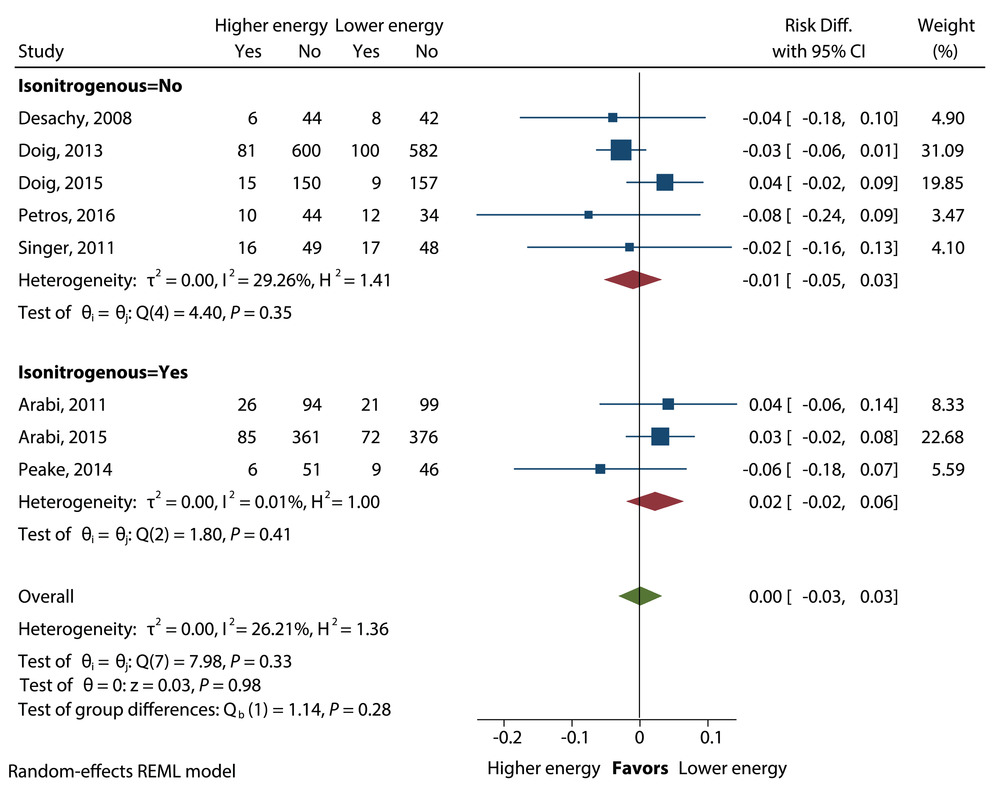
能量摄入量较高与较低的患者在重症监护室死亡率的平均差异。差异,差异;REML,限制性最大似然。
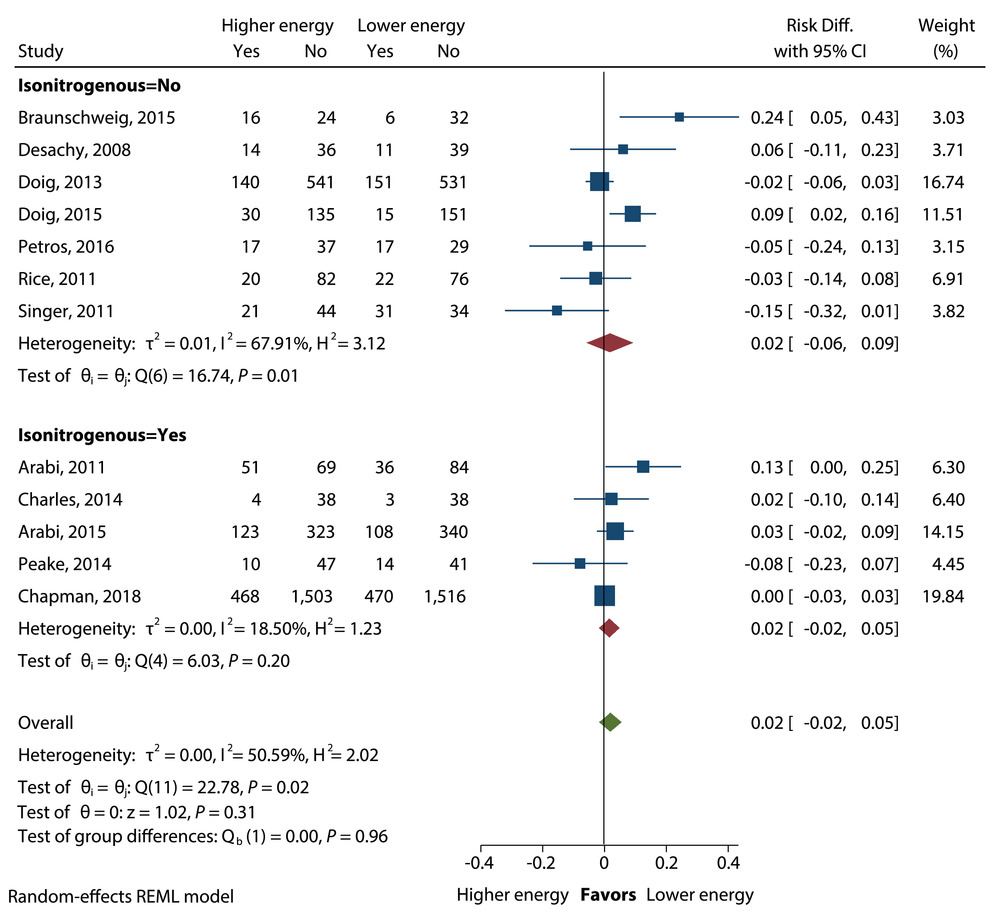
能量摄入较高与较低的患者住院死亡率的平均差异。Diff.,差异;REML,限制性最大似然。
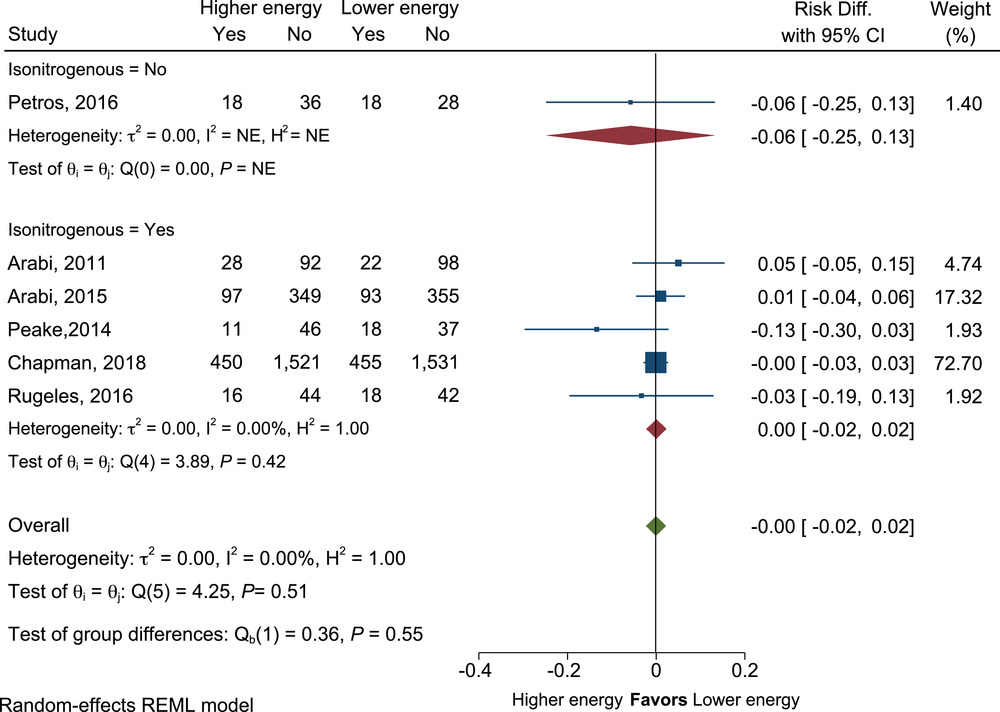
能量摄入较高与较低的患者 28 天死亡率的平均差异。差异,差异;NE,无法估计;REML,限制性最大似然。
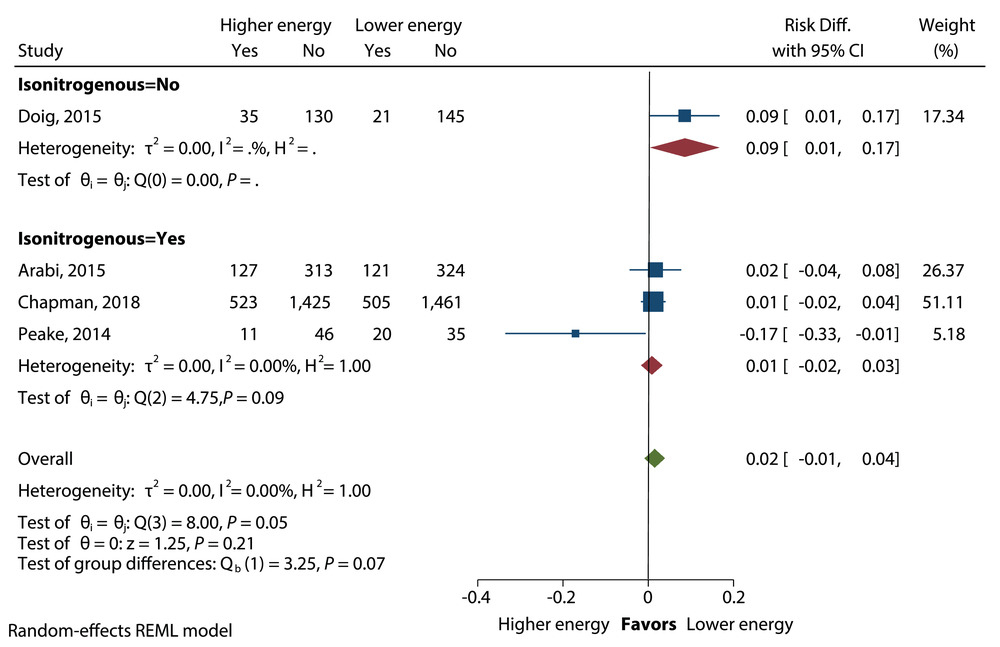
高能量摄入与低能量摄入患者 90 天死亡率的平均差异。差异,差异;NE,不可估计;REML,限制性最大似然。
高能量摄入组与低能量摄入组的肺炎风险没有差异(RD=0.01;95% CI,-0.01 至 0.02;P=0.48),相对于等氮摄入与非等氮摄入,发现不明显(图 3)。
在能量摄入较高与较低的患者中,任何感染的风险都没有不同(RD=0.01;95% CI,-0.04 至 0.05;P=0.74),包括按等氮或非等氮喂养分开的组(图 4)。
高能量组与低能量组的平均 ICU 住院时间没有差异(RD=0.19;95% CI,-1.62 至 2.00 天;P=0.84),包括按等氮状态没有差异(图 5)。
住院时间在低组和高组之间没有差异(RD=-0.88;95% CI,-4.89 至 3.14 天;P=0.67),不考虑等氮饲养(图 6)。
平均呼吸机天数在喂养能量较高与较低的病人之间没有差异(RD = 2.05;95% CI,-1.33 至 5.43 天;P = 0.23)(图 7)。由于只有一个等氮和两个非等氮的试验,亚分析没有意义。
ICU 的死亡率在高喂养或低喂养的干预组中没有差异(RD=0.00;95% CI,-0.03 至 0.03;P=0.98),不管是等氮或非等氮喂养(图 8)。
医院死亡率在高喂养或低喂养的干预组中没有差异(RD=0.02;95% CI,-0.02 至 0.05;P=0.31),不管是等氮还是非等氮喂养(图 9)。
第 28 天的死亡率在高喂养或低喂养的干预组中没有差异(RD=-0.00;95% CI,-0.02 至 0.02;P=0.51)(图 10)。
到第 90 天的死亡率在高喂养或低喂养的干预组中没有差异(RD = 0.01;95% CI,-0.01 至 0.04;P = 0.27)(图 11)。
有四项试验 4、10、12、16 提供了关于 ICU 和 / 或住院时间以及机械通气天数的数据,但无法进行统计学比较,因此没有将这些结果列入林图。这四项研究的结果均无明显差异,表明纳入这些研究不可能改变上述结果的效应大小。
这一建议与本指南的上一版本不同,在上一版本中,根据营养风险或 ARDS 给出了不同的指导 1。以前的指南建议对低营养风险的患者不要进行专门的营养治疗,对有 ARDS 的患者赞成营养性或全剂量 EN,对高营养风险的患者赞成在 48-72 小时内达到估计能量需求的 80% 以上。这是基于这样的理论,即病人对营养的需求会因营养风险评分而不同。到目前为止,这一点既没有通过 RCT 数据得到支持,也没有被反驳。考虑到这一点,以及目前的指南没有发现相对于能量摄入的统计学或临床学上的显著差异,我们选择在本指南中不保留这种营养风险的区分。另外值得注意的是,虽然 2016 年指南中没有报告纳入临床试验的患者的平均 BMI,但本问题所包括的过去 20 年的试验报告的平均 BMI 处于超重或肥胖范围(表 3)。
尽管进行了广泛的研究,但所提供的能量以及如何定义高喂养组和低喂养组方面的不一致抑制了有意义的临床推断。为了比较试验,至少干预组和比较组需要在不同的研究中相似。表 3 显示,在高喂养组中提供 25-30 千卡 / 公斤 / 天的试验,其比较组是不可比的,有两项试验 10、12 的低喂养组所获得的能量水平与大多数其他研究中的高喂养组相当。在如此高的异质性下,除了在危重病人中多喂与少喂的平均相对效果外,不能推断出其他任何东西。安全性分析通过将研究分成随机组,并将其每公斤的能量摄入量与医院死亡率作对比来解决这个问题。该分析报告的一致正斜率与医院(图 8)和 ICU 死亡率(图 9)森林图的一致方向性相结合,即使在对预期干预措施与标准治疗相比是减少(图 S1)还是增加(图 S2)能量摄入进行分层后,也是我们对更高水平能量摄入的安全性缺乏确定性的基础。由于缺乏 RCTs 提供关于暂停喂食后果的数据,加上危重病人的能量消耗和代谢需求增加,我们目前无法推荐暂停喂食。安全性分析意味着迫切需要更多严格控制的能量干预试验,检查较高(25-30 千卡 / 公斤 / 天)的能量暴露与较低(<12-15 千卡 / 公斤 / 天)的影响。这可能需要使用 SPN 或 PN,因为胃部对 EN 的不耐受在危重病人中很常见,并且常常限制了较高能量的提供。现在可能也是时候考虑在精心挑选的人群中进行喂养试验,其中对照组接受非常低或没有营养。这样的研究需要精心设计,以减少伤害,但会提供关于营养支持有效性的宝贵信息。
# 问题 2. 在成人危重病人中,提供较高和较低的蛋白质摄入量是否会影响临床结果?
建议。在相对有限的数据中,临床结果没有差异。由于高质量证据的试验太少,除了 2016 年指南建议的 1.2-2.0g/kg/day 外,我们目前不能提出新的建议。
证据的质量。低
建议的强度。弱
要纳入本问题的分析,试验需要 (1) 报告每天每公斤的蛋白质摄入量(不仅仅是目标的百分比),(2) 组间蛋白质摄入量的差异至少为 0.2 克 / 公斤 / 天,以及 (3) 组间能量摄入量大致相当。为了区分蛋白质供应的影响和不同的能量或微量营养素供应,需要期望有相等的能量摄入。四项试验 18-21 符合这些标准,有 697 名患者的数据(表 4)。
表 4. 问题 2 的数据摘要:在成人危重病人中,提供较高与较低的蛋白质摄入量是否影响临床结果?
| 第一作者,年份 | 人口 | 高蛋白与低蛋白的比较(n)。 | 提供的摄入量 | 感染,n (%) | 机械通气时间,中位数(IQR)或平均 ±SD,天数 | 住院时间,中位数(IQR)或平均 ±SD,天数 | 死亡率,n (%) |
|---|---|---|---|---|---|---|---|
| Doig, 201518 | 16 个内 / 外科 ICU 的患者平均 BMI:28.9 vs 29.5 | IVAA 至 2g/kg/day + 标准治疗(n = 239) vs 标准治疗(n = 235) | 总能量(千卡 / 公斤 / 天)。NRICU 住院期间的蛋白质(g/kg/day):最多 2 vs NR | NR | 每 10 个 ICU 日 7.3(7-7.7) vs 7.3(6.9-7.6)a | ICU:a 11.6 (10.8-12.5) vs 10.7 (10-11.5) 医院:a 26 (24.2-28) vs 24.8 (23-26.6) | ICU:28 (12) vs 30 (13) 医院:a 37 (16) vs 43 (18) 90 天:42 (18) vs 47 (20) |
| Ferrie, 201619 | 内 / 外科 ICU 中需要 PN 的患者 BMI:NR | 1.2 g/kg PN(n = 59)vs 0.8 g/kg PN(n = 60)。 | 7 天的能量(千卡 / 公斤 / 天):23.1±3.9 vs 24.9±4.27 天内的蛋白质(克 / 公斤 / 天)。1.1 ± 0.2 vs 0.9 ± 0.2 | NR | 2.0(1.0-3.0) vs 2.0(1.0-5.0) | 重症监护室。5 (3-8) vs 6 (3.8-10) 医院:25(16.8-41.3) vs 27.5(18.8-55.8) | 重症监护室:8 (14) vs 6 (10) 医院:12 (20) vs 9 (15) 6 个月。15 (25) vs 9 (15) |
| Fetterplace, 201821 | 内科 ICU 的患者平均 BMI:30 vs 29 | 1.5 g/kg EN(n = 30) vs 1.0 g/kg EN(n = 30) | 总能量(千卡 / 公斤 / 天):21±5.2 vs 18±2.7 蛋白质(克 / 公斤 / 天):1.2 ± 0.3 vs 0.8 ± 0.1 | NR | 6.2(4.5-10.8) vs 5.1(3.6-8.5) | ICU:7.8 (5.9-13.4) vs 7.5 (4.9-12.7) 医院:22 (9.9-43) vs 15 (9.9-25) | 28 天:4 (13) vs 5 (17) 60 天:4 (13) vs 5 (17) |
| van Zanten,201820 | 内科、外科或创伤诊断的超重 ICU 患者(BMI≥25)。平均 BMI:30.3 vs 30.7 | 高蛋白 EN(n = 22) vs 标准蛋白 EN(n = 22) | 能量(千卡 / 公斤 / 天):16.6(8.9-23.3) vs 14.4(10.9-18.8) 蛋白质(克 / 公斤 / 天):1.3(0.7-1.9) vs 0.7(0.5-0.9) | NR | 10±8.7 vs 7.4±5.4 | ICU。18.4 ± 13.4 vs 18.3 ± 12.7 医院:28.5 ± 13.3 vs 28.2 ± 13.2 | ICU: 1 (5) vs 2 (9) 医院:2 (9) vs 3 (14) |
- 缩略语。BMI,体重指数(kg/m2);EN,肠内营养;ICU,重症监护室;IVAA,静脉注射氨基酸;Med,医疗;NR,未报告;PN,肠外营养;外科,外科。
对于报告每天每公斤提供的蛋白质的试验,随机到较高蛋白质组的病人的摄入量从 1.119 到 1.3 克 / 公斤 / 天不等。20 Doig 等人 18 的最大试验没有具体报告病人喂养的摄入水平,但 Doig 规定的静脉注射氨基酸剂量估计约为 1.75 克 / 公斤 / 天。所有的试验都提供了可比较的能量摄入。
各项试验的证据质量不同。许多试验没有描述研究设计的细节。然而,有两项试验的样本量较小,而且是为了达到增加蛋白质 20 或蛋白质 / 能量 21 摄入量的主要目的,而不是死亡率,这种结果需要更大的样本量。因此,下面的 ICU 死亡率结果是根据 < 85 个事件报告的,医院死亡率是根据 < 115 个事件报告的。呼吸机天数以平均数 ±SD,20 平均数 / 10 ICU 天数,18 和中位数(IQR)21,19 的形式报告,因此无法合并成一个汇总统计。大多数试验也报告了高蛋白组的 LOS 结果为空,只有一项研究(Fetterplace 等人 21)报告了高蛋白组的住院时间增加。然而,对这一发现的解释受到非异源性随机分组的影响。尽管从逻辑上讲,这些短期结果可能会受到蛋白质摄入水平的影响,但结果的高变异性没有留下可辨别的模式。死亡率数据不足(我们的关键结果)和问题 1 中讨论的同样的间接性问题,使得证据质量等级必须为低。基于可用于评估益处和危害的有限数据,该建议的强度评级为弱。
在三项试验中,637 名患者的数据在 ICU 中没有差异(RD=-0.01;95% CI,-0.06 至 0.04;P=0.81)(图 12)。
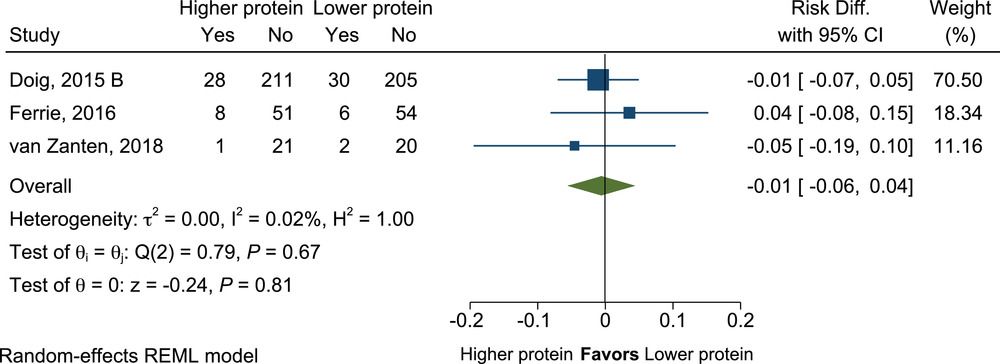
蛋白质剂量较高与较低的病人在重症监护室死亡率的平均差异。Diff.,差异;REML,限制性最大似然。
在三项试验中,637 名患者的数据中,医院死亡率没有差异(RD=-0.02;95% CI,-0.07 至 0.04)(图 13)。
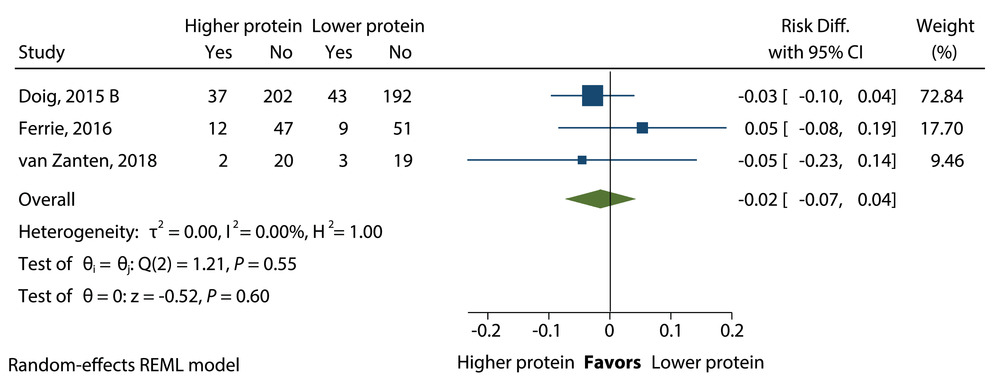
蛋白质剂量较高与较低患者的医院死亡率的平均差异。Diff.,差异;REML,限制性最大似然法
2016 年 ASPEN-SCCM 指南 1 建议大多数重症患者的蛋白质剂量为 1.2-2g/kg/ 天,并建议为烧伤、肥胖或创伤患者提供更高的蛋白质剂量。我们目前的指南是由有限的关于不同蛋白质摄入量的影响的 RCT 数据驱动的。没有发现专门针对烧伤、肥胖或多发性创伤患者的试验符合纳入标准。
目前有几项正在进行的临床试验在危重病人中测试较高与较低的蛋白质剂量(见辅助附录)。假设这些试验在较高与较低的蛋白质剂量下,两组的能量摄入量大致相当,那么很快就会有数据可以更好地指导危重病人的最佳蛋白质供给。
# 问题 3:在成人危重病人中,在危重病人的第一周,PN 与 EN 作为主要喂养方式的能量摄入相似,是否会影响临床结果?
建议。在危重病的第一周,早期纯 PN 和 EN 在临床结果上没有明显差异。由于没有发现 PN 优于 EN,也没有发现伤害的差异,我们建议 PN 或 EN 都可以接受。
证据的质量。高
建议的强度。强烈建议
要纳入本问题的分析,试验需要在 ICU 入院的前 3 天内,将候选 EN 的患者随机分配到 EN 或 PN。两项大型多中心试验比较了早期 PN 和 EN,使用了 4798 名重症内科 ICU 患者的数据,符合我们的纳入标准(表 5)22,23。
表 5. 问题 3 的数据摘要:在成人危重病人中,在危重病的第一周,早期 PN 与 EN 相比,是否会影响临床结果?
| 第一作者,年份 | 人口 | PN 与 EN 的比较(样本量 n)。 | 提供的摄入量 | 感染,n (%) | 机械通气时间,中位数(IQR)或平均 ±SD,天数 | 住院时间,中位数(IQR)或平均数 ±SD,天数 | 死亡率,n (%) |
|---|---|---|---|---|---|---|---|
| 哈维,2014 年 22 | 33 个内科 / 外科重症监护室非计划入院的重症成年人 BMI 中位数:27.7 vs 28.2 | PN(n = 1191) vs EN(n = 1197) | 能量(千卡 / 公斤 / 天):21.3(7.7) vs 18.5(7.7) 总蛋白质(克 / 公斤 / 天)通过 5 天。3±2 vs 3±2 | NR | NR | ICU:8.1 (4-15.8) vs 7.3 (3.9-14.3) 医院:17 (8-34) vs 16 (8-33) | 30 天:393 (33) vs 409 (34) 重症监护室。317 (27) vs 352 (29) 医院: 431 (36) vs 450 (38) 90 天:442 (37) vs 464 (39) |
| Reignier, 201723 | 44 个内科 / 外科 ICU 中需要 PN 的休克的通风成人平均 BMI:27.7 vs 28 | PN(n = 1208) vs EN(n = 1202) | 总能量(千卡 / 公斤 / 天):19.6±5.3 vs 17.8±5.5 vs 蛋白质(克 / 公斤 / 天):0.8(0.2) vs 0.7(0.2) | 菌血症:55 (5%) vs 38 (3%) 肺炎:118 (10%) vs 113 (9%) 任何感染。194 (16%) vs 173 (14%) | NR | ICU。10 (5-17) vs 9 (5-16) 医院:18 (9-33) vs 17 (8-32) | ICU: 405 (31) vs 429 (33) 医院: 479 (34) vs 498 (36) 28 天:422 (35) vs 443 (37) 90 天:507 (43) vs 530 (45) |
- 缩略语。BMI,体重指数(kg/m2);EN,肠内营养;ICU,重症监护室;Med,医疗;NR,未报告;PN,肠外营养;外科,外科。
这个问题的研究质量很高(图 S73-S74)。这两项试验都是为了直接回答我们的问题。他们在入院后 36 小时内 22 或插管后 24 小时内随机选择 PN 或 EN23。然而,报告的结果是从随机到出院;报告的死亡率是到出院后 90 天。没有提供短期干预间隔之外的营养摄入信息。在这些试验中,能量和蛋白质的提供非常相似,这表明观察到的差异不可能是由于其接触的变化。在比较 EN 和 PN 的研究中,盲法是困难的;然而,对于作为主要终点的客观结果测量(死亡率或培养证明的感染)来说,这种缺乏盲法的影响可能很小。22, 23 这两项大型试验中的高样本量和低偏差研究设计,以及它们一致的发现,支持证据质量为高。未来不太可能进行大型试验来回答这个问题。建议等级为强,因为在选择使用 EN 与 PN 方面似乎没有任何危害或益处。鉴于这些数据,与临床结果的差异相比,提供 EN 与 PN 的成本和便利性可能是危重病早期喂养途径的更大决定因素。
由于只有两项试验,所以不可能对森林图中的数据进行比较以评估效果大小。表 5 总结了各个试验的结果。没有报告任何临床结果的显著差异。感染等不良事件没有明显差异,如预期的那样,肠道喂养不耐受在 EN 治疗组更常见。
没有发现不同模式之间的优越性,也没有发现在危重病人早期提供短程 PN 会增加感染或其他不良事件。
这一建议与之前的指南不同。基于专家的共识,2016 年 ASPEN-SCCM 指南建议对无法耐受 EN 的低营养风险患者暂停使用 PN7 天,但对高营养风险患者或营养不良患者使用 PN。目前的指南是基于最新的(2001-2020 年)、来自大型多中心试验的更高质量的数据。在危重病人中更现代的营养支持做法,包括改进导管护理、血糖控制和避免过度喂食能量,可能已经减少了早年使用 PN 时常见的菌血症和高血糖的风险。目前的试验也是在 ICU 入院后 24-36 小时内开始喂食,并持续几天,而不是几周或更长时间。因为本建议所依据的证据主要是在 ICU 入院的前 3 天内开始 PN,并且只持续治疗 5-7 天,所以本建议是针对 ICU 治疗的第一周和可能是 EN 的候选人的患者。鉴于这些研究中不能耐受 EN 的患者人数有限,其结果可能无法推广到 EN 耐受性下降的患者群体中,如复杂的手术人群。
# 问题 4. 在接受早期 EN 的成人危重病人中,提供 SPN 以满足能量目标与在危重病的第一周不提供 SPN 相比,是否会影响临床结果?
建议。在临床结果方面没有明显差异。基于在 ICU 入院早期提供 SPN 没有临床意义的发现,我们建议在 ICU 入院的第 7 天之前不要开始提供 SPN。
证据的质量。高
建议的强度。强烈建议
为了纳入本问题的分析,试验需要报告 SPN 与无 SPN 或标准治疗的结果差异。六项 RCTs17, 25-29,数据来自 6731 名危重病人,符合我们的纳入标准(表 6)。
表 6. 问题 4 的数据摘要:在接受早期 EN 的成人危重病人中,在危重病的第一周提供 SPN 以满足能量目标与不提供 SPN 是否影响临床结果?
| 第一作者,年份 | 人口 | SPN 与对照组的比较(样本量 n)。 | 提供的摄入量 | 感染,n (%) | 机械通气时间,中位数(IQR),天数 | 住院时间,中位数(IQR)或平均值 ±SD,天数 | 死亡率,n (%) |
|---|---|---|---|---|---|---|---|
| 阿林斯特鲁普。201726 (opens new window) | 急性住院的成人 ICU 患者 BMI 中位数:22 vs 22 | 在 ICU 住院期间,通过间接量热法添加 PN(n = 100)vs 25 kcal/kg EN(n = 99)的剂量 | 能量(千卡 / 天):1877(1567-2254) vs 1061(745-1470)。蛋白质(克 / 公斤 / 天):1.5(1.1-1.7) vs 0.5(0.3-0.7) | 菌血症:5 (5) vs 4 (4) 肺炎:4 (4) vs 4 (4) 任何感染。19 (19) vs 12 (12) | NR | ICU:7 (5-22) vs 7 (4-11) 医院。30 (12-53) vs 34 (14-53) | 28 天:20 (20) vs 21 (21) 90 天:30 (30) vs 32 (32) 6 个月。37 (37) vs 34 (34) |
| Casaer, 201129 | 营养风险评分≥3 分(满分 7 分)的患者;40% 紧急入院 BMI≥25,57.3% vs 55.7 | 早期 PN(n = 2312) vs 延迟 PN(n = 2328)(两组同时接受 EN) | NR | 菌血症:174(7.5) vs 142(6.1) 肺炎:447(19.3) vs 381(16.4) 任何感染。605 (26.2) vs 531 (22.8) | 2(1-5) vs 2(1-5) | ICU。4 (2-9) vs 3 (2-7) 医院。NR | ICU: 146 (6) vs 141 (6) 医院:251 (11) VS 242 (10) 90 天:255 (11) vs 257 (11) |
| Doig, 201317 | 31 个内科 / 外科 ICU 中对 EN 有短期禁忌的重症患者平均 BMI:27.9 vs 28.5 | 早期 PN(n = 681) vs 标准治疗(n = 682)(两组都接受 EN)。 | NR | 菌血症:39 (6) vs 33 (5) 肺炎:43 (6) vs 45 (7) 任何感染。74 (11) vs 78 (11) | NR | ICU: a8.6 (8.2-9) vs 9.3 (8.9-9.7) 医院:A25.4(24.4-26.6) vs 24.7(23.7-25.8) | ICU:81 (12) vs 100 (15) 医院:140 (21) vs 151 (22) 60 天:146 (22) vs 155 (23) |
| Heidegger, 201325 | 内 / 外科 ICU 的患者平均 BMI:25.4 vs 26.4 | EN+SPN 以满足需求(n = 153) vs 单独 EN(n = 152) | 能量(千卡 / 公斤 / 天),第 4-8 天:28 ± 5 vs 20 ± 7 蛋白质(克 / 公斤 / 天),第 4-8 天:1.2 ± 0.2 vs 0.8 ± 0.3 | 菌血症:10 (19) vs 6 (14) 肺炎:35 (67) vs 28 (65) | 6.4±6.8 vs 6.9±6.7 | ICU。13±10 vs 13±11 医院。31±23 vs 32±23 | ICU: 8 (5) vs 12 (7) 医院:20 (13) vs 28 (18) |
| Ridley, 201827 | 病情危急的成年人平均 BMI:29 vs 30 | ICU 第 3 天入院时,EN+SPN(n = 51) vs 单独 EN(n = 48) | 能量(千卡 / 公斤 / 天):24.9±6.4 vs 16.8±8.2 蛋白质(克 / 公斤 / 天):1.0 ± 0.3 vs 0.6 ± 0.3 | 任何感染。18 (35) vs 16 (33) | 10(6-15) vs 8(5-18) | ICU。11 (5-17) vs 11 (6-17) 医院:22±21 vs 23±17 | ICU: 15 (29) vs 11 (23) 医院:16 (31) vs 11 (23) 90 天:19 (37) vs 13 (27) 180 天:19 (37) vs 13 (27) |
| Wischmeyer, 201728 | 体重不足和肥胖的危重病成人平均 BMI:33.5 vs 33.2 | EN + SPN (n = 52) vs EN (n = 73) | NR | 菌血症:0 vs 1 (2.2) 肺炎:12(31.6) vs 18(39.1) 任何感染。14 (26.9) vs 23 (31.5) | 6.5(3.9-14.1) vs 8.3 (3.8-13.3) | ICU。12.8 (7.9-17.8) vs 12.6 (8.1-18.7) 医院:23.5(17.5-34.7) vs 24(16.6-38.9) | ICU:7 (14) vs 13 (18) 医院:8 (15) vs 17 (23) |
- 缩略语。BMI,体重指数(kg/m2);EN,肠内营养;ICU,重症监护室;Med,医疗;NR,未报告;PN,肠外营养;SPN,补充 PN;外科,外科。
证据的质量是不同的。所有的试验都在研究登记时使用了随机化隐蔽性,客观的主要结果,以及盲目的结果判断者。然而,有两项试验 27 和 28 将蛋白质或能量输送作为主要结果,有一项试验 26 侧重于生活质量。大多数报告了急性 ICU 入院情况,但最大的试验 30 只登记了 40% 的急性入院病人。三项试验 17、28、29 没有报告提供能量或蛋白质的数量,而其他试验则记录了 SPN 组更多的能量和蛋白质摄入。对 ICU 和住院时间以及呼吸机使用天数的研究结果的表述方法不一,使我们无法确定这些结果的效应大小,而且报告的结果也各不相同。大多数试验报告了机械通气天数以及 ICU 和住院时间的无效结果。一个例外是大型的 EPaNIC 研究 29(n = 4640),该研究报告了 ICU 寿命的延长和需要机械通气 2 天以上的病人的百分比增加。根据我们的关键结果 -- 医院死亡率,这组试验的证据质量很高。对这个问题的推荐力度是强的。
添加 SPN 后,ICU 住院期间的结果没有明显改善。菌血症的风险没有明显差异(RD=0.01;95% CI,-0.00 至 0.02;P=0.18),标准治疗组的菌血症风险为 6%(图 14)。
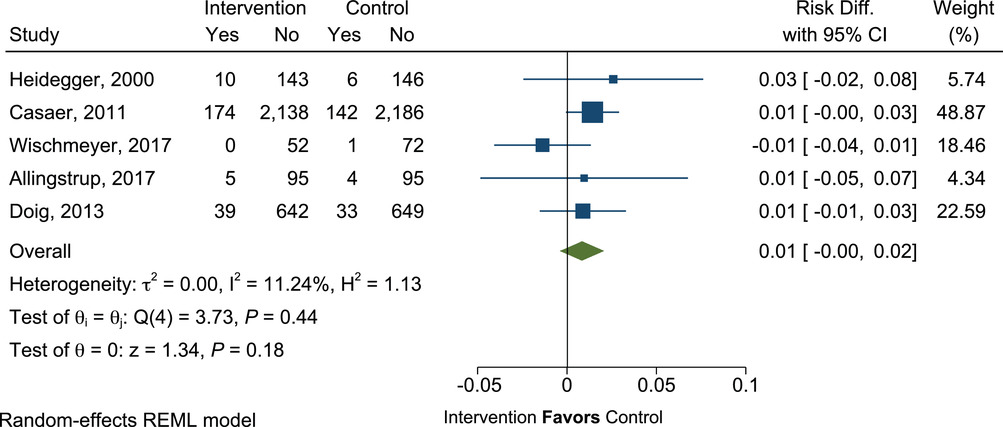
有补充肠外营养(PN)的重症患者与无补充 PN 的重症患者的菌血症发生率的平均差异。Diff.,差异;REML,限制性最大似然。
添加 SPN 后,肺炎的发生率没有差异(RD=0.01;95% CI,-0.01 至 0.04;P=0.36),对照组的肺炎风险为 17%(图 15)。
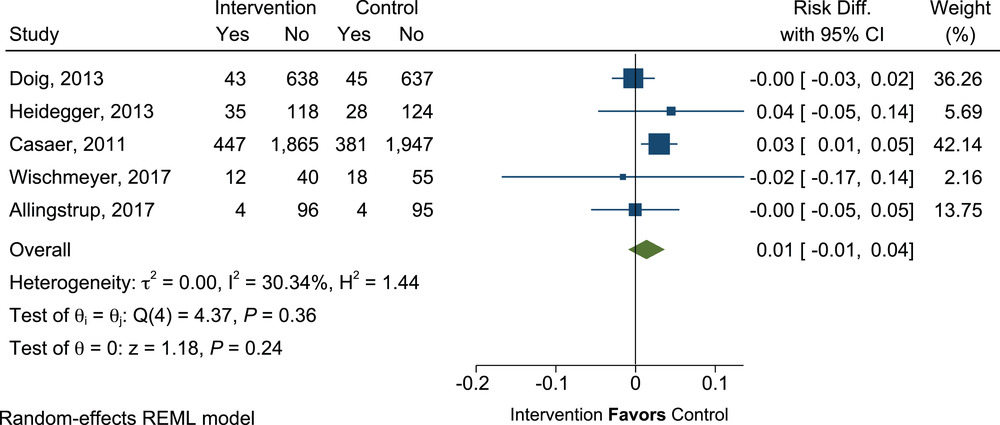
有补充肠外营养(PN)的重症患者与没有补充 PN 的重症患者肺炎发病率的平均差异。Diff.,差异;REML,限制性最大似然。
任何类型的感染与添加 SPN 没有区别(RD=0.02;95% CI,-0.01 至 0.05;P=0.25),对照组的任何感染率为 20%(图 16)。
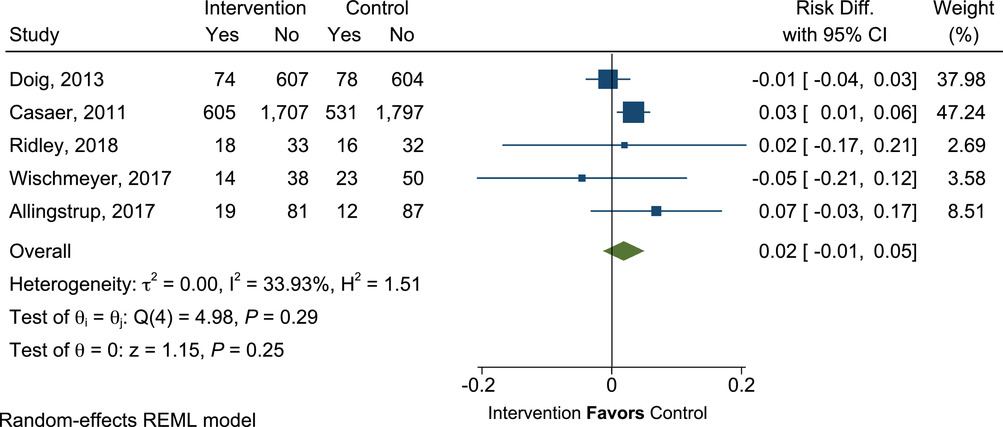
有补充肠外营养(PN)的重症患者与无补充 PN 的重症患者任何感染的平均差异。Diff.,差异;REML,限制性最大似然法
在包括 6532 名患者数据的 5 项试验中,添加 SPN 后 ICU 死亡率没有差异(RD=-0.01;95% CI,-0.03 至 0.01;P=0.42),对照组的 ICU 死亡率为 8%(图 17)。
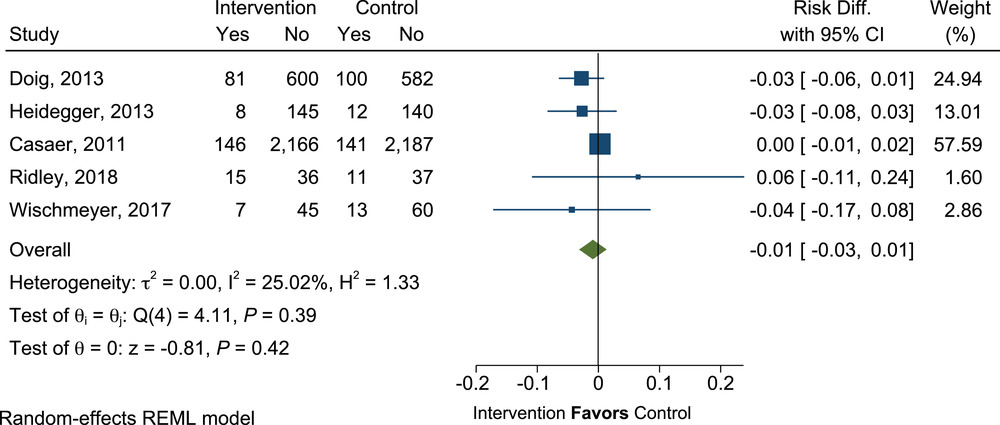
使用补充肠外营养(PN)与不使用补充 PN 的危重病人在重症监护室死亡率的平均差异。Diff.,差异;REML,限制性最大似然法
在 5 项试验中,6532 名患者的数据中,添加 SPN 的医院死亡率没有差异(RD=-0.00;95% CI,-0.03 至 0.02;P=0.69),对照组的医院死亡率为 14%(图 18)。
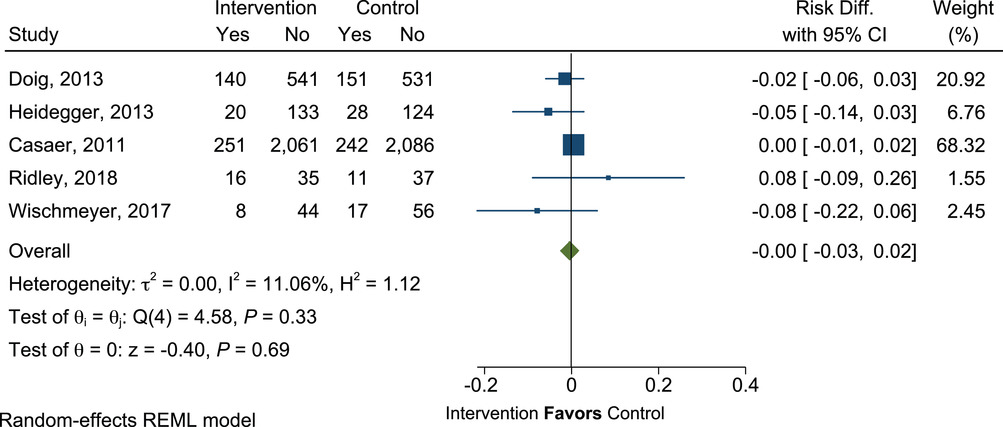
有补充肠外营养(PN)的危重病人与没有补充 PN 的危重病人住院死亡率的平均差异。Diff.,差异;REML,限制性最大似然法
添加 SPN 后的 90 天死亡率没有差异(RD=0.00;95% CI,-0.02 至 0.02;P=0.96),对照组的 90 天死亡率为 12%(图 19)。
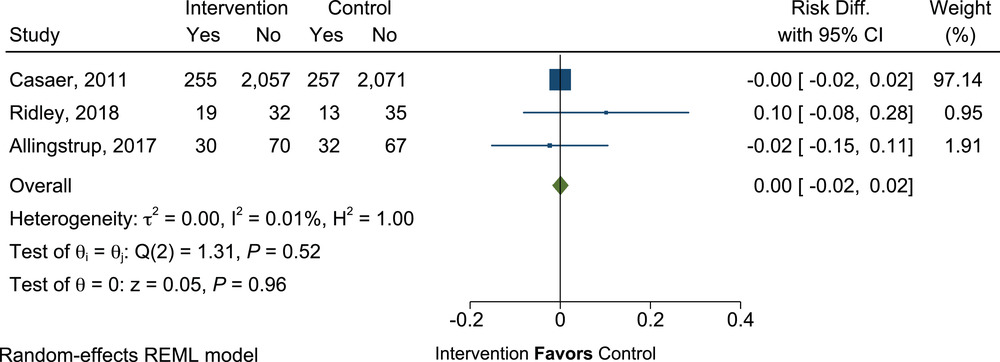
有补充肠外营养(PN)的重症患者与没有补充 PN 的重症患者 90 天死亡率的平均差异。Diff.,差异;REML,限制性最大似然法
以前的指南建议,对于无法耐受 > 60% 目标蛋白质和能量需求的患者,在 7-10 天后使用 SPN。1, 24 而 2016 年的指南建议等待 7-10 天再添加 SPN,这里包括的试验在第 3 天就开始使用 SPN,并且大多数持续治疗 6-8 天。然而,在综合数据中没有注意到感染性并发症或死亡率的差异。基于在 ICU 入院早期提供 SPN 没有临床意义的发现,我们建议在 ICU 入院第 7 天之前不要开始使用 SPN。
# 问题 5A. 在接受 PN 的成人重症患者中,提供多种油 ILE(即中链甘油三酯、橄榄油、FO、多种油),与 100% SO ILE 相比,是否会影响临床结果?
建议。由于关键结果的统计学或临床学上的差异有限,我们建议向适合启动 PN 的重症患者提供多种油 ILE 或 100% SO ILE,包括在进入 ICU 的第一周。
证据的质量。低
建议的强度。弱
要纳入本问题的分析,RCTs 需要 (1) 比较使用多种油 ILE 和 100% SO ILE 作为 PN 的组成部分来启动 PN,(2) 报告临床结果。七项试验 31-37 符合这些标准,有 624 名患者的数据(表 7)。
表 7. 问题 5A 的数据摘要:在接受 PN 的成人重症患者中,提供多种油 ILE(即 MCTs、OO、FO、油的混合物),与 100% SO ILE 相比,是否会影响临床结果?
| 第一作者,年份 | 人口 | 多种油与对照组的比较(样本量 n)。 | 提供的摄入量 | 感染,n (%) | 呼吸机天数,平均值 ±SD | 住院时间,中位数(IQR),天数 | 死亡率,n (%) |
|---|---|---|---|---|---|---|---|
| Chen, 201732 | 1 个 ICU 中的 SIRS 患者 BMI: NR | PN 提供 20 千卡 / 千克 / 天,10 克 FO/50 克 SO ILE(n = 24) vs PN 与 SO ILE(n = 24)。 | 能量(千卡 / 公斤 / 天)。NR 蛋白质(克 / 公斤 / 天)。NR | NR | NR | ICU。13.8 ± 9.9 vs 24.4 ± 23.2 | 28 天:3(13)对 10(42)。 |
| Donoghue,201931 | 外科 ICU 的 ARDS 或 SIRS 平均 BMI:29.2 vs 27.6 | PN 与 30% SO/30% MCT/25% OO/15% FO ILE(n = 35)vs 100% SO ILE(n = 33)。 | 能量(千卡 / 公斤 / 天)。NR 蛋白质(克 / 公斤 / 天)。NR 四种油类 ILE: 0.09-0.22 g/kg/day | NR | 1.24 ± 0.83 vs 0.88 ± 1.63 | ICU:9.5 ± 7.1 vs 10.7 ± 7.6 | NR |
| Metry, 201433 | 外科 ICU 的术后患者平均 BMI:27.9 vs 28.1 | 含 30% SO/30% MCT/25% OO/15% FO ILE 的 PN(n = 41) vs 含 100% SO ILE 的 PN(n = 42) | 能量(千卡 / 公斤 / 天):35 vs 35 蛋白质(克 / 公斤 / 天):1.2 vs 1.2ILE(克 / 千克 / 天):1.2+0.3 FO vs 1.5 | NR | 6.5 ± 5.1 vs 7.2 ± 4.3 | ICU。10.4 ± 6.2 vs 11.7 ± 7.2 医院:15.7±11.4 vs 19.4±12.6 | 30 天:3 (7) vs 3 (7) |
| Sabater, 201134 | ARDSBMI:NR | 10%FO/50%MCT/40%SO ILE(n = 8) vs 100%SO ILE(n = 8) | 能量(千卡 / 公斤 / 天)。NR 蛋白质(克 / 公斤 / 天)。NRILE (g/kg/day): NR | NR | NR | NR | 医院。4 (50) vs 2 (25) |
| Umpierrez, 201235 | 成人内外科 ICU 患者平均 BMI:27.4 vs 27.3 | 80% OO/20% SO ILE 的 PN(n = 49)vs 100% SO ILE 的 PN(n = 51) | 能量(千卡 / 公斤 / 天):22±6 vs 22±5 蛋白质(克 / 公斤 / 天)。1.2 ± 0.3 vs 1.2 ± 0.3ILE(g/kg/day):0.6 ± 0.2 vs 0.6 ± 0.2 | 菌血症:11 (22) vs 11 (22) 肺炎:7 (14) vs 5 (10) 任何感染:29 (57) vs 21 (43) | NR | 重症监护室。17±18 vs 15.2±14 医院。40.8 ± 36 vs 46.7 ± 48 | 重症监护室。4 (8) vs 5 (10) 医院:5(10) vs8 (16) |
| Weiss, 200236 | 成人外科 ICU 患者 BMI:NR | PN 达 1400 千卡,10 克 FO/50 克 SO(n = 12)vs 50 克 SO(n = 11)。 | NR | 肺炎:1 (8) vs 3 (27) | NR | 重症监护室。4.1 vs 9.1 医院:17.8 vs 23.5 | 医院:1 (8) vs 1 (9) |
| Wichmann, 200737 | 腹部大手术平均 BMI:25 vs 25 | PN 与 10% FO/50% MCT/40% SO ILE(n = 127)vs 100% SO ILE(n = 129)。 | NR | 菌血症:4(3%) vs 5(4%)。肺炎:1(0.8) vs 5(4) | NR | ICU。4.1 vs 6.3 医院:17.2 vs 21.9 | ICU:6(5) vs 3(2) |
- 缩略语。ARDS,急性呼吸窘迫综合征;BMI,体重指数(kg/m2);FO,鱼油;ICU,重症监护室;ILE,脂质注射乳剂;MCT,中链甘油三酯;Med,医疗;NR,未报告;OO,橄榄油;PN,肠外营养;SIRS,全身炎症反应综合征;SO,豆油;外科,外科。
所有配方都与 100% SO ILE 进行了结果比较;但是,干预组有很大的不同。在两项试验中,干预措施是 30% SO/30% 中链甘油三酯(MCT)/25% 橄榄油(OO)/15% FO ILE31, 33;在两项试验中,10% FO/50% MCT/40% SO ILE34, 37;在两项试验中,50 克 SO/10 克 FO ILE32, 36;以及在一项试验中,80% OO/20% SO ILE35,干预时间从 12 小时 34 到 28 天不等。这些研究在开始时将 ILE 作为 PN 方案的一部分,而不是根据 2016 年指南中非常低质量的证据建议在第一周暂停使用。
报告的任何临床结果都没有差异,而且试验之间的证据质量普遍较低。没有计划进行以研究本指南所选临床结果为主要目的的试验。两项试验 31,33 没有使用 ITT 分析或分析试验完成者和非完成者之间的差异。大多数试验 31、32、34、36、37 对能量或干预措施的报告不清楚。没有一项试验是针对死亡结果的。只有两项试验 31, 33 报告了机械通气的天数。每个结果的事件数量都很有限(肺炎,22 起;菌血症,31 起;ICU 死亡率,18 起;医院死亡率,21 起;28 天 / 30 天死亡率,19 起)。较低的事件发生率可能使许多研究没有足够的能力来检测效果。严重的偏倚风险和缺乏对关键结果的力量,导致该问题的证据质量等级为低。由于缺乏高质量的证据,无法确定危害和益处,因此对该问题的推荐力度较弱。
2016 年 ASPEN-SCCM 指南中没有及时收录多种油 ILE 产品 1。目前对重症患者的 RCT 研究有限,需要进一步研究多种油 ILE 的潜在抗炎和免疫调节特性。鉴于临床结果的差异在统计学上或临床上不明显,我们建议目前可以向适合开始使用 PN 的重症患者提供多种油 ILE 或 100% SO ILE,包括在 ICU 入院的第一周。
# 问题 5B. 在接受 PN 的成人重症患者中,提供含 FO 的 ILE 与不含 FO 的 ILE 相比,是否会影响临床结果?
建议。因为只有一项结果有显著差异,而其他关键的下游结果没有数据支持,所以我们建议向适合开始使用 PN 的重症患者提供含 FO 或不含 FO 的 ILE,包括在 ICU 入院的第一周。
证据的质量。低
建议的强度。弱
要纳入本问题的分析,RCT 需要(1)比较含 FO 的 ILE 和不含 FO 的 ILE 作为 PN 的组成部分,以及(2)报告相关的临床结果。10 项试验 31-34, 36-41 符合这些标准,共有 919 名患者的数据(表 8)。在这些研究中,ILE 在开始使用时被作为 PN 方案的一部分。
表 8. 问题 5B 的数据摘要:在接受 PN 的成人危重病人中,与不含 FO 的 ILE 相比,提供 FO 的 ILE 是否影响临床结果?
| 第一作者,年份 | 人口 | FO 与对照组的比较(样本量 n)。 | 提供的摄入量 | 感染,n (%) | 呼吸机天数,平均值 ±SD | 住院时间,中位数(IQR),天数 | 死亡率,n (%) |
|---|---|---|---|---|---|---|---|
| Barbosa, 2010038 | 单一中心研究中患有 SIRS 的成人平均 BMI:28.9 vs 28.5 | 10%FO/50%MCT/40%SO(n = 13) vs 50%MCT/50%SO(n = 10) | 能量(千卡 / 公斤 / 天):29.3±7.6 vs 25.3±5.6 蛋白质(克 / 公斤 / 天):1.17 ± 0.30 vs 1.22 ± 0.28 | NR | 10±4 vs 11±4 | ICU。12 ± 4 vs 13 ± 4 医院:22±7 vs 55±16 | 28 天:4(31) vs 4(40) |
| Chen, 201732 | 单一中心的 SIRS 患者 BMI:NR | PN 提供 20 千卡 / 千克 / 天,10 克 FO/50 克 SO ILE(n = 24) vs PN 与 SO ILE(n = 24)。 | 能量(千卡 / 公斤 / 天)。NR 蛋白质(克 / 公斤 / 天)。NR | NR | NR | ICU: 13.8 ± 9.9 vs 24.4 ± 23.2 | 28 天:3(13)对 10(42)。 |
| Chen, 201739 | 患有严重脓毒症、机械通气和急性消化道功能障碍的成人 BMI:NR | 提供 10 克 / 天 FO 的 PN(n = 41)vs 标准 PN(n = 37),持续 7 天 | NR | NR | NR | NR | 28 天:10 (24) vs 15 (41) 60 天:11 (27) vs 18 (49) |
| Donoghue, 201931 | 外科 ICU 的 ARDS 或 SIRS 平均 BMI:29.2 vs 27.6 | 使用 30% SO/30% MCT/25% OO/15% FO/ ILE 的 PN(n = 35)vs 100% SO ILE(n = 33),为期 6 天 | 能量(千卡 / 公斤 / 天)。NR 蛋白质(克 / 公斤 / 天)。NR 四种油的 ILE:0.09-0.22 克 / 公斤 / 天 | NR | 1.2 ± 0.8 vs 0.9 ± 1.6 | ICU:9.5 ± 7.1 vs 10.7 ± 7.6 | NR |
| Friesecke, 200841 | 成人内科 ICUBMI:NR | 83% Lipofundin(50% MCT/50% SO)+17% Omegaven(FO 乳液)(n = 83)vs 100% Lipofundin(n = 82)。 | 能量(千卡 / 公斤 / 天):22.2 ± 5.5 vs 21.6 ± 5.6 蛋白质(克 / 公斤 / 天):1.1 ± 0.3 vs 1.1 ± 0.3 脂质(克 / 公斤 / 天):0.91±0.26 vs 0.93±0.28 | 肺炎:4 (5) vs 5 (6) | 22.8 ± 22.9 vs 20.5 ± 19.0 | ICU:28±25 vs 23±20 | 28 天:18 (22) vs 22 (27) |
| Grau-Carmona, 201540 | 17 个内科 / 外科 ICU 的成人平均 BMI:26.6 vs 27.1 | 10% FO/50% MCT/40% SO(n = 81)vs 50% MCT/50% SO(n = 78),持续 5 天 | 能量(千卡 / 天):1737 vs 1782 蛋白质(克 / 公斤 / 天):1.43 vs 1.41 血脂(克 / 公斤 / 天):1.04 vs 1.05 | 菌血症:10 (12) vs 12 (15) 肺炎:7 (11) vs 14 (22) | a7(6.0) vs 8(8.5) | ICU: a 12 (18.5) vs 18 (13.25) 医院:a25 (34.5) vs 36.5 (34.0) | 重症监护室:26 (33) vs 16 (21) 医院。32 (44) vs 22 (31) 6 个月。34 (42) vs 24 (31) |
| Metry, 201433 | 外科 ICU 的术后患者平均 BMI:27.9 vs 28.1 | 使用 30% SO/30% MCT/25% OO/15% FO ILE 的 PN(n = 41)vs 使用 100% SO ILE 的 PN(n = 42),为期 7 天 | 能量(千卡 / 公斤 / 天):35 vs 35 蛋白质(克 / 公斤 / 天):1.2 vs 1.2ILE(克 / 千克 / 天):1.5+0.3 FO vs 1.5 | NR | 7.2 ± 4.3 vs 6.5 ± 5.1 | ICU。10.4 ± 6.2 vs 11.7 ± 7.2 医院:15.7±11.4 vs 19.4±12.6 | 30 天:3 (7) vs 3 (7) |
| Sabater, 201134 | ARDSBMI:NR | 10% FO/50% MCT/40% SO ILE(n = 8) vs 100% SO ILE(n = 8),持续 12 小时 | NR | NR | NR | NR | 医院。4 (50) vs 2 (25) |
| Weiss, 200236 | 成人外科 ICU 患者 BMI:NR | PN 达 1400 千卡,10 克 FO/50 克 SO(n = 12)vs 50 克 SO(n = 11)。 | NR | 肺炎:1 (10) vs 3 (14) | NR | 重症监护室。4.1 vs 9.1 医院:17.5 vs 23.5 | 医院:1 (8) vs 1 (9) |
| Wichmann, 200737 | 腹部大手术平均 BMI:25 vs 25 | PN 与 10% FO/50% MCT/40% SO ILE(n = 127)vs 100% SO ILE(n = 129)。 | NR | 菌血症:4(3) vs 5(4) 肺炎:1(0.8) vs 5(4) | NR | ICU。4.1 vs 6.3 医院:17.2 vs 21.9 | ICU:6(5) vs 3(2) |
- 缩略语。ARDS,急性呼吸窘迫综合征;BMI,体重指数(kg/m2);FO,鱼油;GI,胃肠道;ICU,重症监护室;ILE,脂质注射乳剂;Med,医疗;MCT,中链甘油三酯;NR,未报告;PN,肠外营养;SIRS,系统性炎症反应综合征;SO,豆油;外科,外科。
这些试验的证据质量普遍较低。大多数试验主要集中在生化或炎症结果上。没有一项研究将本指南中考虑的临床结果作为其主要结果,所有结果都报告了少量的事件。两项试验 31、33 没有使用 ITT 分析。大多数试验 31、32、34、36、37、39、40 在报告能量和 / 或提供的干预方面不明确。所有的配方都与不含 FO 的 ILE 进行了结果比较;但是,干预组的情况有很大的不同。干预的时间一般都很短,尤其是相对于结果的时间框架而言。与问题 5A 一样,严重的偏倚风险和缺乏关键结果的力量,导致该问题的证据质量等级为低。由于缺乏高质量的证据,无法确定其危害和益处,因此对该问题的建议强度为弱。
图 20-25 代表了以可比方式报告数据的研究。除肺炎外,含 FO 或不含 FO 的 ILE 在任何临床结果方面都没有发现明显的效果差异。接受 FO ILE 的患者的肺炎减少。然而,这一发现并没有得到下游变量(如机械通气天数或 LOS)的无效结果的支持(图 21)。因此,这些发现并不影响建议。其他感染、ICU 死亡率和住院时间的数据也是以一种方式报告的,无法估计汇总统计和生成森林图。
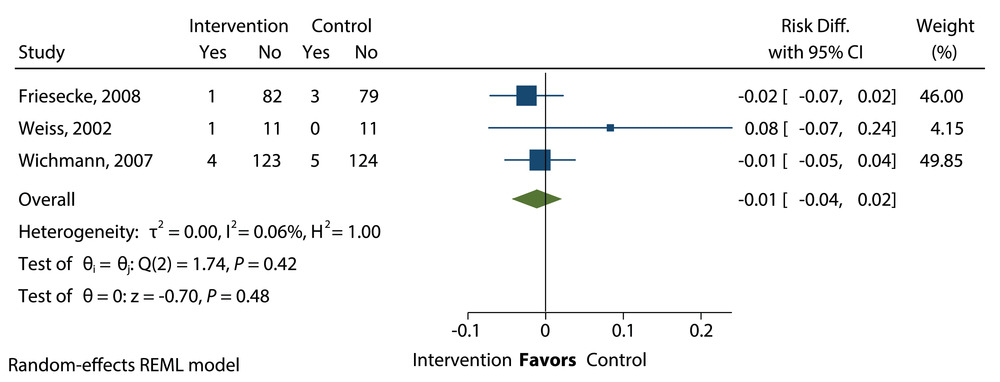
接受含鱼油(FO)的脂质注射乳剂(ILE)的重症患者与不含鱼油的 ILE 的导管相关感染发病率的平均差异。Diff.,差异;REML,限制性最大似然。
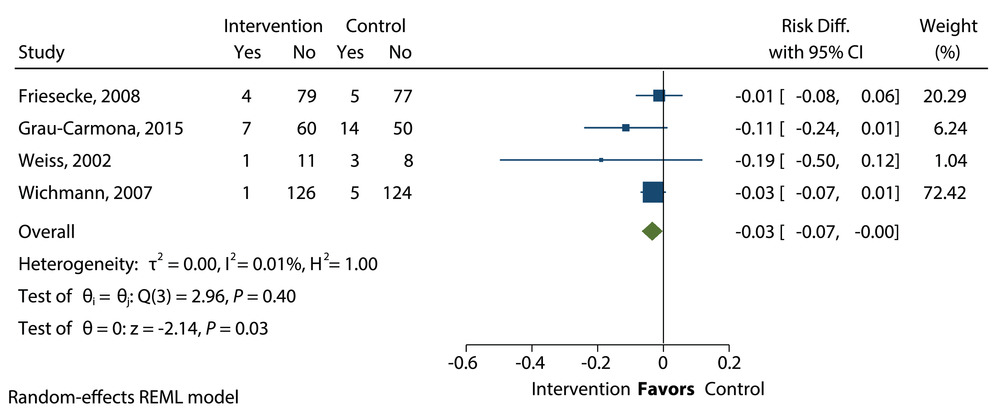
接受含鱼油(FO)的脂质注射乳剂(ILE)与不含鱼油的 ILE 的重症患者肺炎发病率的平均差异。Diff.,差异;REML,限制性最大似然。
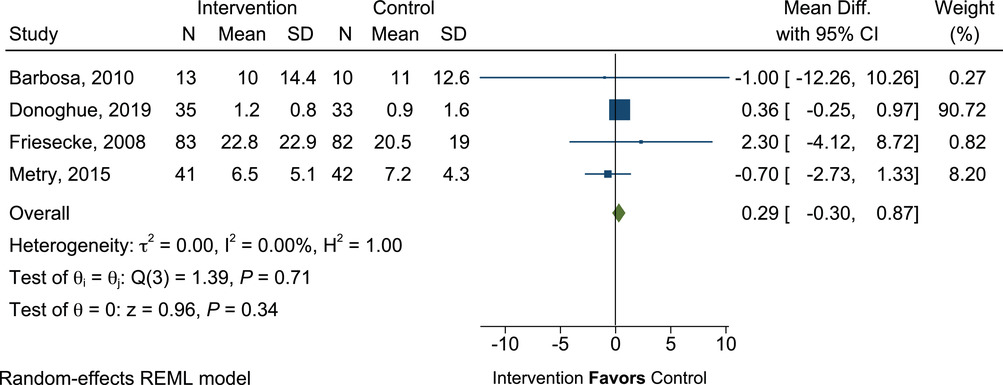
接受含鱼油(FO)的脂质注射乳剂(ILE)的重症患者与不含鱼油的 ILE 的机械通气天数的平均差异。Diff.,差异;REML,限制性最大似然法
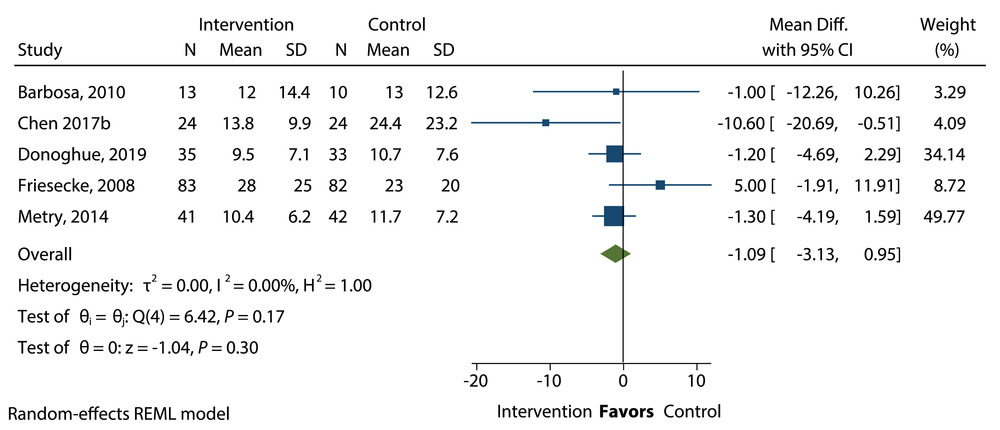
接受含鱼油(FO)的脂质注射乳剂(ILE)与不含鱼油的 ILE 的危重病人在重症监护室停留时间的平均差异。Diff.,差异;REML,限制性最大似然。
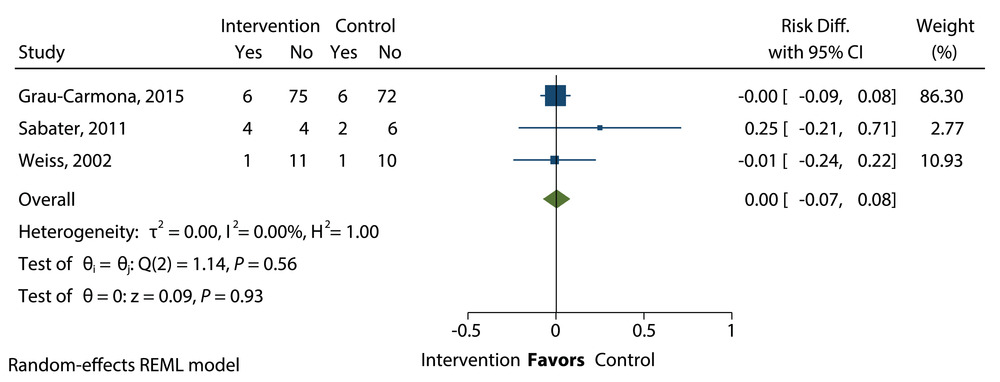
接受含鱼油(FO)的脂质注射乳剂(ILE)与不含鱼油的 ILE 的危重病人的医院死亡率的平均差异。Diff.,差异;REML,限制性最大似然。
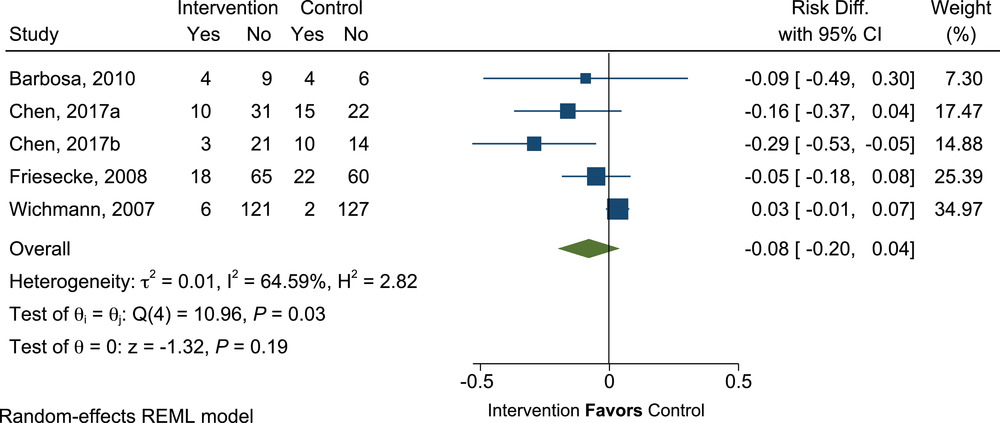
接受含鱼油(FO)的脂质注射乳剂(ILE)的重症患者与不含鱼油的 ILE 的 30 天死亡率的平均差异。差异,差异;REML,限制性最大似然。
在包括 469 名患者数据的三项试验中,接受含 FO 与不含 FO 的 ILE 的患者的导管相关感染发生率没有差异(RD=-0.01;95% CI,-0.04 至 0.02 天;P=0.48),而对照组的导管相关感染风险为 3.7%(图 20)。
在包括 575 名患者数据的四项试验中,接受含 FO ILE 的患者与不含 FO ILE 的患者相比,肺炎的发生率有所下降,共发生了 40 起事件(RD=-0.03;95% CI,-0.07~0.00 天;P=0.03)。FO ILE 组的肺炎风险为 5%∼,非 FO ILE 组为 9%∼(图 21)。这一结果有利于 FO 干预,可以认为具有临床意义,但由于研究数量少,而且研究结果没有得到其他应该因肺炎事件而恶化的无效结果的支持,如机械通气天数和 ICU LOS,因此对这一估计的信心受到一定程度的抑制。出于这个原因,决定推荐 FO 为时尚早。未来的研究将揭示出 FO ILE 的初步受益信号是否保持,这个问题将被重新审视。
在包括 339 名患者数据的四项试验中,接受含 FO 与不含 FO 的 ILE 的患者机械通气天数没有差异(RD=0.29;95% CI,-0.30 至 0.87 天;P=0.34),对照组的平均机械通气时间为 9.9 天(图 22)。不幸的是,只有 Friesecke 等人 41 同时报告了肺炎和机械通气时间。
在包括 387 名患者数据的五项试验中,接受含 FO 与不含 FO 的 ILE 的患者的 ICU LOS 没有差异(RD = -1.09;95% CI,-3.13 至 0.95 天;P = 0.3),对照组的平均 ICU LOS 为 16.6 天(图 23)。
在包括 198 名患者数据的三项试验中,接受含 FO 与不含 FO 的 ILE 的患者的医院死亡率没有差异(RD=0.00;95% CI,-0.07 至 0.08;P=0.93),对照组的医院死亡率为 12.5%(图 24)。
在包括 570 名患者数据的五项试验中,接受含 FO 与不含 FO 的 ILE 的患者一个月的死亡率(28 天和 30 天)没有区别(RD=-0.08;95% CI,-0.20 至 0.04;P=0.19),对照组的死亡率为 18.8%(图 25)。
基于这些发现,我们建议向适合开始使用 PN 的重症患者提供含 FO 或不含 FO 的 ILE,包括在进入 ICU 的第一周。考虑到肺炎的初步受益信号,显然需要进行更多的研究来阐明含 FO 的 ILE 在 PN 配方中的作用。
# 其他问题
尽管我们最初搜索了与八个问题有关的试验,但只找到了符合纳入和排除标准的 RCTs 来回答作者提出的上述五个问题。没有找到足够的数据来解决作者团队一开始就确定的三个重要的重症监护营养问题。
- 在成人危重病人中,较高的营养风险分数是否比单独作为营养风险指标的 BMI 预测更差的结果?我们的搜索结果显示,没有任何 RCT 研究比较根据重症患者营养风险(NUTRIC)评分或 2002 年营养风险筛查(NRS2002)工具随机分组的患者相对于 BMI 的临床结果。迄今为止,支持这些营养评估方法的证据主要是基于回顾性的观察性研究,这种证据水平在本指南中被排除。
- 在成人危重病人中,增强免疫力的营养素是否比标准治疗提供更好的结果?这个广泛的问题包含了不同数量的营养素(谷氨酰胺;ω-3 脂肪酸;个别维生素、矿物质和微量元素),这些营养素的剂量变化很大。由于本指南的重点是为普通重症患者的基础实践问题提供答案,因此决定在未来构建一个作者小组,将这个问题作为自己的指南来处理。
- 在成人危重病人中,益生菌是否比标准治疗提供更好的结果?我们的搜索策略所确定的 RCTs 报告了各种益生菌制剂和剂量,并没有对本指南所包括的结果进行一致的报告。
# 未来的研究方向
尽管考虑了许多设计良好的试验的数据,包括一个有强有力证据的问题,但上述大多数建议都很弱,是根据低到中等质量的证据提出的。死亡率(ICU、医院或 90 天)是这些问题中最具可比性的结果,尽管在治疗的第一周后出现的死亡率可能很难与早期有时间限制的营养支持干预措施明确挂钩。诸如住院时间和呼吸机天数等结果可能会受到喂养决定的影响。不幸的是,关于这些结果的报告差异很大,降低了混淆研究结果的能力。缺乏有关营养暴露变量的报告(每天每公斤获得的能量和每天每公斤获得的蛋白质克数)进一步限制了我们回答大多数问题的能力。下面列出的项目为改善未来 ICU 营养支持的研究提供了建议,并增加了我们对最佳营养护理的认识。
- 营养状况可能会影响 ICU 的结果,在未来的重症监护营养研究中应该考虑到这一点。遗憾的是,营养状况往往没有被评估,而当它被包括在内时,不同的研究对它的定义往往是不同的。有许多工具可以评估营养状况。全球营养不良领导小组(GLIM)的标准是努力将所有这些工具收集成一套标准,以方便不同工具之间的比较。42 GLIM 标准提出营养不良的诊断应基于三个表型标准中的至少两个(非季节性体重减轻、低 BMI、肌肉量减少)和两个病因学标准中的至少一个(食物摄入 / 吸收减少或疾病负担增加)。为了研究的目的,我们建议研究将 GLIM 标准数据包括在他们的表格或补充资料中,以方便进行荟萃分析。对于未来在 ICU 人群中的研究,我们建议 (1) 针对营养状况的黄金标准,如瘦肉状况的放射成像,对 GLIM 工具进行验证研究;(2) 在基线数据中包括 GLIM 标准的 RCT,并衡量营养干预对不同营养状况水平的临床结果的影响。这将大大改善围绕这一工具的效用的科学性,并将使文献中充斥着可用于统计混淆的可比性研究。
- 营养支持疗法为患者提供针对能量和蛋白质目标的营养物质。为了评估营养支持的影响,研究者必须报告提供给患者的所有主要暴露变量的数量(对于本临床指南,能量、蛋白质或 ILE 的数量)。为了能够在试验之间进行准确的比较,并确定最佳的喂养方法,这些变量应该以每公斤的热量、每公斤的蛋白质或每公斤体重的 ILE 克数为标准来报告,数据为平均值 ±SD。此外,应明确说明体重是如何获得的。
- 应描述整个结果观察期间的营养摄入量。总的来说,在 ICU 人群中进行的大多数营养试验都很短(5-7 天或仅在机械通气期间),报告的许多结果包括 RCT 间隔后发生的措施(例如,住院时间、死亡率、试验后感染)。这些干预后的结果反映了在试验期间接受的营养以及试验后的间隔,即所有参与者都恢复到标准的营养护理(即所有患者的喂养方式与对照组相似)。如果营养摄入确实影响试验后的结果,那么较长的干预后持续时间将减弱这些结果在各组之间的差异。此外,相对较短的试验时间并没有提供任何关于更广泛、更有参考价值的问题,即旨在优化整个住院期间的营养护理的综合方法如何影响短期和长期的医院结果。
- 本指南使用的许多结果是以中位数(IQR)报告的,因此不能与以平均值 ±SD 报告的数据相结合。试验应以中位数(IQR)以及平均数 ±SD 报告 LOS 和呼吸机天数的数据,以便在森林图中比较所有试验,根据平均数 ±SD 确定效应大小。如果在主文件中倾向于中位数(IQR),这些数据可以在在线补充表格中公布。
- 到目前为止,还没有临床试验研究在危重病人中暂停与提供非自愿性喂食的影响。仍然需要包括极低至无营养摄入的研究设计,以充分探索非传统喂养的临床疗效。
- 在危重病人中,可能受到营养支持影响的其他临床结果包括再次入住重症监护室或医院、体力或表现的测量、出院处置(康复与持续护理、有协助的家庭与没有添加疗法的家庭)和 / 或重症监护后综合症的发生率。评估和报告这些结果的标准化方法应该是一个优先事项,以便能够对这些结果的干预措施进行有力的检测。
