 嗜铬细胞瘤和副神经节瘤诊断治疗专家共识 ( 2020 版)
嗜铬细胞瘤和副神经节瘤诊断治疗专家共识 ( 2020 版)
# 嗜铬细胞瘤和副神经节瘤诊断治疗专家共识 (2020 版)
中华医学会内分泌学分会。嗜铬细胞瘤和副神经节瘤诊断治疗专家共识 (2020 版)[J]. 中华内分泌代谢杂志,2020,36 (9):737-750.
| 本共识中常见英文缩略语释义 | ||
|---|---|---|
| 缩略语 | 英文全称 | 中文全称 |
| 3-MT | 3-methoxytyramine | 3 - 甲氧基酪胺 |
| CA | Catecholamine | 儿茶酚胺 |
| DA | Dopamine | 多巴胺 |
| E | Epinephrine | 肾上腺素 |
| FDG | Fluorodeoxyglucose | 脱氧葡萄糖 |
| 11PLC | High performance liquid chromatography | 高效液相色谱法 |
| HPLC-ECD | High performance liquid chromatography with electrochemical detection | 高效液相色谱电化学检测法 |
| 11VA | Homovanillic acid | 高香草酸 |
| LC-ECD | Liquid chromatography-electrochemical detection | 液相色谱电化学检测法 |
| LC-MS/MS | Liquid chromatography tandem mass spectrometry | 液相色谱串联质谱法 |
| MIBG | Metaiodobenzylguanidine scintigraphy | 间碘苄基胍 |
| MN | Metanephrine | 甲氧基肾上腺素 |
| MNs | Metanephrine and normetanephrine | 甲氧基肾上腺素类 |
| NE | Norepinephrine | 去甲肾上腺素 |
| NMN | Normetanephrine | 甲氧基去甲肾上腺素 |
| PCC | P heochromocytoma | 嗜铭细胞瘤 |
| PET/CT | Positron emission tomography/computer tomography | 正电子发射计算机断层扫描 |
| PGL | Paraganglioma | 副神经节瘤 |
| PPGL | P heochromocytoma and paraganglioma | 嗜铭细胞瘤和副神经节瘤 |
| SDH | Succinate dehydrogenase | 琥珀酸脱氢酶 |
| SPECT | Single-photon emission computed tomography | 单光子发射计算机断层成像 |
| VMA | Vanillylmandelic acid | 香草扁桃酸 |
# 本共识依据
为规范嗜铬细胞瘤 (pheochromocytoma,PCC) 及副神经节瘤 (paraganglioma,PGL) 的诊断和治疗,中华医学会内分泌学分会肾上腺学组 2016 年发表了专家共识 [1]。 根据近年来在分子遗传学、表观遗传学、肿瘤病因学、靶向药物及基因治疗等方面的快速发展, 现修订并发表 2020 版中华医学会内分泌学分会专家共识。
本共识采用国际上通用的表述推荐强度及证据质量的方法。 (1) 推荐强度:“强烈推荐” 使用 “推荐” 及数字 1 表示,即按此处理利大于弊;“一般推荐” 使用 “建议” 和数字 2 表示,即依据患者情况决定最佳个体化方案。 (2) 证据质量:●○○○,表示极低证据质 量;●●○○,表示低证据质量;●●●○,表示中等证据质量;●●●●,表示高证据质量。
# 本共识要点
1. 推荐:对以下人群进行嗜铬细胞瘤和副神经节瘤 (pheochromocytoma and paraganglioma, PPGL) 筛查 (1|●●●●)。
◆有 PPGL 症状和体征,有阵发性高血压发作、伴头痛、心悸、多汗三联征、体位性低血压的患者。 ◆服用多巴胺 (dopamine, DA) 受体拮抗剂、拟交感神经类、阿片类、去甲肾上腺素 (norepinephrine,NE) 或 5 - 羟色胺再摄取抑制剂、单胺氧化酶抑制剂等药物诱发 PPGL 症状发作。 ◆肾上腺意外瘤。 ◆有 PPGL 或 PPGL 相关遗传综合征家族史。 ◆有 PPGL 既往史。
2. 推荐:诊断 PPGL 首选血浆游离或尿液甲氧基肾上腺素类 (metanephrine and normetanephrine, MNs) 浓度测定 (1|●●●●);建议:可同时检测血或尿 NE、肾上腺素 (epinephrine, E)、DA 和其他代谢产物 3 - 甲氧基酪胺 (3-methoxytyramine, 3-MT)、高香草酸 (homovanillic acid, HVA) 和香草扁桃酸 (vanillylmandelic acid, VMA) 浓度以帮助诊断 (2|●●●○)。
3. 推荐:首选使用液相色谱串联质谱法 (liquid chromatography tandem mass spectrometry, LC-MS / MS) (1|●●●●) 测定 MNs;建议:使用液相色谱电化学检测法 ( liquid chromatography-electrochemical detection, LC-ECD) 测定 MNs,高效液相色谱电化学检测法 (high performance liquid chromatography with electrochemical detection, HPLC-ECD) 测定 NE、E 和 DA (2|●●●○)。
4. 推荐:首选计算机断层扫描 (computer tomography, CT) 作为肿瘤定位的影像学检查 (1|●●●○);推荐:磁共振成像 (MRI) 用于探查颅底和颈部 PGL、 已有肿瘤转移、体内存留金属异物、对 CT 显影剂过敏、儿童、孕妇等需要减少放射性暴露的人群 (1|● ●●○)。
5. 建议:有转移或不能手术的 PPGL 患者先做,131I - 间碘苄基胍 (metaiodobenzylguanidine, MIBG) 核素显像 (国外用123I-MIBG),根据肿瘤的功能和解剖定位来评价131I-MIBG 治疗的可能性 (2|●●●○)。
6. 推荐:所有 PPGL 患者均应到正规实验室进行基因检测,对所有转移性 PPGL 患者应检测琥珀酸脱氢酶 (succinate dehydrogenase, SDH) B 基因 (1 | ●●● ○);建议:根据肿瘤定位和儿茶酚胺 (catecholamine, CA) 生化表型选择不同类型的基因检测 (2| ●●● ○);对有 PPGL 阳性家族史和遗传综合征表现的患者可直接检测相应的致病基因突变 (2|●●●○)。
7. 推荐:除头颈部副交感神经性 PGL 和分泌 DA 的肿瘤外,其余患者应先用肾上腺素能 α- 受体阻滞剂做术前准备 (1|●●●○);推荐:对大多数 PCC 行腹腔镜微创手术,对肿瘤直径 > 6 cm、侵袭性 PPGL 进行开放式手术 (1|●●●○);推荐:对 PGL 行开放式手术 (1|●● ○○);建议:对双侧 PCC 应采取保留部分皮质的肾上腺切除术 (cortex sparing adrenalectomy)(2|●●○○)。
8. 推荐:术后 24~48 h 密切监测患者的血压和心率 (1|●●○○);PPGL 患者需终身随访,推荐每年至少复查 1 次;有基因突变、转移性 PPGL 患者应 3~6 个月随访 1 次,对其直系亲属应检测基因和定期检查 (1 |●●●○)。
# 相关定义和流行病学特征
# 一、相关定义
# (一) PCC 及 PGL
PCC 是起源于肾上腺髓质,PGL 是起源于肾上腺外的交感神经链并具有激素分泌功能的神经内分泌肿瘤,主要合成、分泌和释放大量 CA,如 NE、E 和 DA,引起患者血压升高和代谢性改变等一系列临床症候群, 并造成心、脑、肾、血管等严重并发症甚至成为患者死亡的主要原因。 PCC 肿瘤位于肾上腺,PGL 肿瘤位于胸、腹部和盆腔的脊椎旁交感神经链,二者合称为 PPGL。
来源于沿颈部和颅底分布的舌咽、迷走神经的 PGL 则称为头颈部 PGL,因其来自副交感神经节故通常不产生 CA。 而起源于交感神经副神经节,广泛分布在从颅底到盆腔底并且具有 CA 分泌功能的 PGL 也称为交感神经性 PGL。
# (二) 转移性 PPGL
2017 年世界卫生组织 (WHO) 在神经内分泌肿瘤分类中用 “转移性 PPGL” 替换了 2004 年定义的 “恶性 PPGL”,认为所有的 PPGL 都具有转移潜能,故建议将 PPGL 分类改为转移性和非转移性,而不再用恶性和良性分类。 如果在非嗜铬组织如骨、肝、肺、淋巴结、脑或其他软组织中出现了转移病灶则称为转移性 PPGL。
# (三) PPGL 的 TNM 分期
2017 年美国癌症联合会 (American Joint Committee on Cancer, AJCC) 公布了 PPGL 的第一个临床分期体系,按照肿瘤定位、原发肿瘤形态、功能和有无转移等制订了 TNM 系统 Ⅰ~Ⅳ 分期,但 AJCC 的 TNM 分期目前不包括副交感神经来源的 PGL。
1. T:原发肿瘤形态和部位。 TX,原发肿瘤无法评估;T1,最大径 <5 cm 的肾上腺内肿瘤,无肾上腺外浸润;T2,最大径≥5 cm 的肾上腺内肿瘤,无肾上腺外浸润,或不论大小、但有交感神经功能的肿瘤;T3,不论肿瘤大小但已浸润到周围组织 (肝、胰、脾、肾)。
2. N:区域淋巴结转移。 NX,区域淋巴结无法评估;N0,无局部区域淋巴结转移证据;N1,有局部区域淋巴结转移。
3. M:远处转移病灶。 M0,无远处转移;M1,有远处转移;M1a,仅有转移至骨;M1b,转移至远处淋巴结 / 肝 / 肺;M1c,转移至骨及其他多个部位。
4. PPGL 的 TNM Ⅰ~Ⅳ 分期:Ⅰ 期,T1/ N0/ M0;Ⅱ 期,T2/ N0/ M0;Ⅲ 期,T1/ N1/ M0、T2/ N1/ M0、T3/ N0 或 N1/ M0;Ⅳ 期,T1~3/ N0 或 N1/ M1。
# 二、流行病学特征
PPGL 是一种引起内分泌性高血压的少见神经内分泌肿瘤,目前国内尚无发病率或患病率的确切数据。 国外报道 PCC 的发病率为 2 ~ 8 例 / 百万人每年, 10%~20% 发生在儿童;患者生前未被诊断而在尸检时 PPGL 的检出率为 0.05%~0.1%。
PPGL 在普通高血压门诊中患病率为 0.2% ~ 0.6%,在儿童高血压患者中为 1.7%,在肾上腺意外瘤中约占 5%。 在 PPGL 肿瘤中 PCC 占 80%~85%、PGL 占 15% ~ 20%;遗传性 PPGL 占 35% ~ 40%;转移性 PPGL 占 10%~17%,转移性肿瘤中 PCC 占 5%~20%, 交感神经性 PGL 占 15%~35%。
PPGL 在各年龄段均可发病,但发病高峰为 30~ 50 岁,男女发病率基本相同。 43% ~ 71% 的成人和 70%~82% 的儿童其转移性 PPGL 发病与编码 SDHB 的基因突变有关。 与散发性患者相比,遗传性 PPGL 患者起病较年轻并呈多发性病灶。
# 临床表现及筛查
# 一、临床表现
PPGL 患者的主要临床表现为 CA 分泌增多所致的高血压及心、脑、肾血管并发症和代谢性改变,由于肿瘤发生在不同部位及持续性或阵发性分泌释放不同比例的 E 和 NE,并与不同亚型的肾上腺素能受体结合起作用,故患者有下述多系统的临床表现。
# (一) 血压变化
高血压是 PPGL 患者的主要临床表现 (90% ~ 100%),可为阵发性 (40% ~ 50%)、持续性 (50% ~ 60%) 或在持续性高血压的基础上阵发性加重 (50%); 约 70% 的患者合并体位性低血压;多数患者表现为难治性高血压,另有少数患者血压可正常。
有的患者可发生高血压危象,PPGL 危象发生率约为 10%,临床表现多样化,如严重高血压、循环衰竭、休克,或高低血压反复交替发作,多器官功能障碍如心肌梗死、心律失常、心肌病和心源性休克;肺水肿和急性呼吸窘迫综合症 (ARDS);脑血管意外、脑病和癫痫;麻痹性肠梗阻和肠缺血、肝肾功能衰竭等,严重者导致死亡。
危象可自发产生,也可因术前或术中挤压触碰肿瘤、创伤、服用某些药物 (糖皮质激素、β- 受体阻滞剂, 胃复安、麻醉药) 或其他手术应激等诱发,应注意尽量避免上述诱因。 PPGL 高血压危象发作时,需静脉泵入 α- 受体阻滞剂 (酚妥拉明或乌拉地尔) 治疗及大量补液以纠正低血压休克。 PPGL 危象死亡率高,需密切监测血压及其他血流动力学指标。
# (二) 三联征
头痛 (59% ~ 71%)、 心悸 (50% ~ 65%)、 多汗 (50%~65%) 是 PPGL 患者高血压发作时最常见的三联征 (40%~48%),对诊断具有重要意义。 如患者同时有高血压、体位性低血压并伴头痛、心悸、多汗三联征则诊断 PPGL 的特异度为 95%。
# (三) 其他的特征性临床表现
由于肾上腺素能受体 α 和 β 的不同亚型可广泛分布于全身多种组织和细胞,故 PPGL 患者有多系统的症状和体征。
1. 心血管循环系统:患者高血压发作时可有心悸、 胸闷、濒死感;有 CA 心肌病的患者可伴发心律紊乱、 Takotsubo 心肌病;有的患者发生心绞痛、急性冠状动脉缺血综合征甚至心肌梗死、低血压休克等。 尸检发现 58% 的 PPGL 患者存在 CA 心肌损害,除了长期严重的高血压能导致心室肥厚外,高 CA 血症能导致心肌损伤及心肌纤维化、心肌缺血和心律失常等。 如明确诊断 PPGL 的患者有胸痛、心力衰竭症状和体征;心电图提示持续 3 个或 3 个以上导联 T 波低平或倒置、 S-T 段偏移或心律失常;超声心动图提示心肌肥厚、左室舒张功能减低、左室射血分数降低,室壁运动异常, 当肿瘤切除后上述病变明显改善或消失,则可考虑 CA 心肌病的诊断。 Takotsubo 心肌病 (又称短暂性左心室心尖球样综合征) 是极罕见的 PPGL 心肌病变,临床表现及心电图与急性心肌梗死相似,左室造影显示室壁运动异常 (心尖部及心室中部运动障碍和心底部的过度收缩) 而无冠状动脉异常。
CA 心肌病导致的心律失常、心力衰竭及心肌梗死是 PPGL 患者术前的常见死因。 手术切除肿瘤后,CA 心肌病患者的心律失常、心肌缺血,心电图及心功能可恢复正常,心室肥厚逆转,但陈旧心肌梗死会长期存在。
2. 消化系统:可有恶心 / 呕吐、腹痛、便秘、肠梗阻、 胆石症等。
3. 泌尿系统:常有血尿、蛋白尿,肾功衰竭等,如为膀胱 PGL 则排尿时有高血压发作及 CA 增多的表现。
4. 神经精神系统:患者表现为头痛、失眠、烦躁、紧张焦虑,有时需要与焦虑症、抑郁、惊恐状态等鉴别;严重时可发生脑血管意外、意识障碍等。
5. 血液系统:可有发热、白细胞增多等。
6. 内分泌代谢系统:可伴有糖、脂代谢紊乱,糖耐量受损或糖尿病 (42% - 58%);常有多汗、体重下降 (23% ~70%)、代谢率增高等表现。
7. 腹部肿物:15% 的患者在查体时可触及到腹部肿瘤并因压迫肿瘤而致血压升高。
# 二、 PPGL 遗传综合征的其他临床表现
遗传学研究表明,不同类型基因突变的 PPGL 患者,在肿瘤部位、非转移性 / 转移性、激素分泌类型、 多发 / 单发 / 复发倾向以及临床表现等方面均有明显差异。
SDH 基因不同亚型胚系突变患者除 PPGL 肿瘤外,还可伴发其他实体瘤如胃肠道间质瘤、肾细胞癌和垂体腺瘤,而称为家族性 PGL 遗传综合征,为常染色体显性遗传性疾病。 依据不同的 SDH 基因亚型而分别命名为 PGL-1 (SDHD)、 PGL-2 ( SDHAF2)、 PGL-3 (SDHC)、PGL-4 ( SDHB) 和 PGL-5 ( SDHA) 五种亚型 (表 1)。
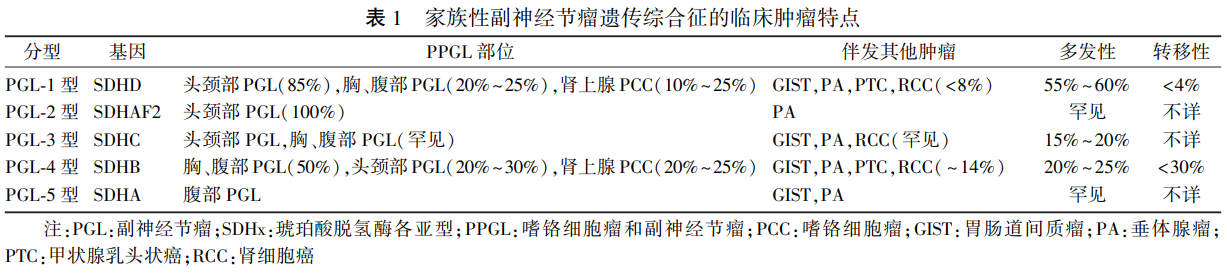
除 PPGL 外其他遗传综合征可包括的临床疾病如下所示。
1. 多内分泌腺瘤病 (MEN) 2A 型:甲状腺髓样癌、原发性甲状旁腺功能亢进症、皮肤淀粉样变性苔藓。
2. MEN 2B 型:甲状腺髓样癌、皮肤黏膜多发神经瘤、骨骼畸形、关节松弛、类马凡体型、角膜神经髓鞘化、肠神经节瘤 (先天性巨结肠病)。
3. 希佩尔 - 林道综合征 (von Hippel-Lindau, VHL 综合征): 除 PCC 外患者可有多器官肿瘤,包括中枢神经系统血管母细胞瘤 (小脑、脊髓、脑干)、视网膜血管母细胞瘤、肾透明细胞癌 / 肾囊肿、胰腺神经内分泌肿瘤和浆液性囊腺瘤,内耳淋巴囊腺瘤、附睾和子宫阔韧带的乳头状囊腺瘤等。
4. 神经纤维瘤病 1 型 (NF1): 全身多发神经纤维瘤、多发牛奶咖啡斑、腋窝和腹股沟斑点、虹膜错构瘤、骨异常、中枢神经系统神经胶质瘤、巨头畸形、认知障碍等。
# 三、 PPGL 筛查对象
推荐:对以下人群进行 PPGL 筛查 (1|●●●●)。
1. 有 PPGL 的症状和体征,特别是有阵发性高血压伴头痛、心悸、多汗三联征、体位性低血压的患者。
2. 服用 DA 受体拮抗剂、拟交感神经类、阿片类、 NE 或 5 - 羟色胺再摄取抑制剂、单胺氧化酶抑制剂等药物而诱发 PPGL 症状发作。
3. 肾上腺意外瘤。
4. 有 PPGL 或 PPGL 相关上述遗传综合征家族史。
5. 有 PPGL 既往史。
# 定性诊断
# 一、 CA 及其代谢产物水平测定
推荐:诊断 PPGL 实验室检查首选血浆游离或尿液甲氧基肾上腺素 (metanephrine, MN)、甲氧基去甲肾上腺素 ( normetanephrine, NMN) 浓度测定 (1 | ●●●●);建议:可同时检测血或尿 NE、E、DA 及其他代谢产物 3-MT、HVA 和 VMA 浓度以帮助诊断 (2 | ●●●○)。
CA 及其中间和终末代谢产物浓度的测定是 PPGL 定性诊断的主要依据,包括测定血 / 尿 CA 原型物质 NE、E、DA,中间代谢产物 NMN、MN (二者总称 MNs)、3-MT,终末代谢产物 VMA、HVA 浓度。
NMN 及 MN 分别是 NE 和 E 的中间代谢产物 (合称 MNs),其仅在肾上腺髓质嗜铬细胞或 PPGL 肿瘤体内代谢生成,并且以高浓度水平持续存在;MNs 的半衰期较 CA 长,也更加稳定,其特异度和灵敏度高,能反映 PPGL 肿瘤的功能状态,故成为 PPGL 诊断指南和共识首先被推荐的特异性标记物。
# (一) MNs 水平测定
建议:用相同体位的正常参考区间来判断测定结果 (2 | ●●○○)。
1. 血浆游离 MNs: 因患者体位及应激状态均可影响 CA 及 MNs 水平,从仰卧位到直立位的血浆 CA 及 MNs 可升高 2 ~ 3 倍 [18-19] ;坐位 NMN 水平的参考值上限是仰卧位的 2 倍 [2] ;故建议患者检测前应仰卧位或坐位至少休息 30 min 后再采血,判断结果时采用相同体位的参考值。
2. 24 h 尿 MNs: 患者应准确留取 24 h 尿量并保持尿液酸化再检测 MNs 水平,尿液酸化至 pH 4.0 可防止 CA 降解,但 pH 低于 2.0 则可增加游离 CA 水平 [20] 。
3. 推荐:首选使用 LC-MS / MS 测定 MNs (1 | ●● ●●);如无质谱分析仪则建议用 LC-ECD 测定 MNs (2 | ●●●○) 。
因 CA 的化学性质不稳定,在检测时需防止其降解;CA 及代谢产物浓度低 (pg/ml),色谱分离难度较大,干扰物较多,故对仪器的灵敏度要求高。 CA 及代谢产物的检测经历了多种方法:生物分析法、比色法,灵敏度较低;荧光法,易受其他内源性化合物干扰;放射酶法,操作繁琐;化学发光法,检测灵敏度不能满足临床检验需要;液相色谱与电化学联用 (LC-ECD),虽然灵敏度和选择性高,但耗时长,也易受到多种物质干扰。 随着质谱技术的快速发展,LC-MS/MS 因其灵敏度高,特异度强,能进行大量样本的快速筛选,目前已成为检测 CA 及代谢产物的主要方法并被指南和共识所推荐。
为保证检测准确性,样本的采集及保存应如下:采血管用乙二胺四乙酸 (EDTA) 或肝素抗凝,血样置于冰水中送到实验室,采血后在 30 min 内于 4℃离心,离心前加入抗氧化剂,血浆放在 - 20℃ 或 - 80℃ 保存待测。 尿液采集中加入 Na2EDTA/ Na2 S2O5 ,收到尿样用盐酸酸化至 pH 4.0,在 4℃ 或 - 18℃ 可保存 10 周。 MNs 比 CA 稳定, 在室温下存储 7 d, 尿液中游离 NMN、MN 的浓度均保持稳定,且不受 pH 值和防腐剂的影响。
目前,国内外关于 CA 及代谢物的质谱法测定结果的一致性在不同实验室还存在很大差异,需要建立统一的室间质量评价参考体系来推动检测标准化。
4. 影响 MNs 测定的因素:应激状态、剧烈运动、吸 烟、饮用咖啡因、酒精类、含酪胺 / CA 类食物等对 CA 及 MNs 测定可导致假阳性结果;一些严重疾病患者在 重症监护时也可出现假阳性结果,故检测前至少 8 h 内应避免上述情况。
5. NMN 水平的年龄变化:NMN 随着年龄增加而升高,而 MN 不随年龄变化,故需按年龄调整 NMN 正常参考值上限,以减少假阳性率 (表 2)。
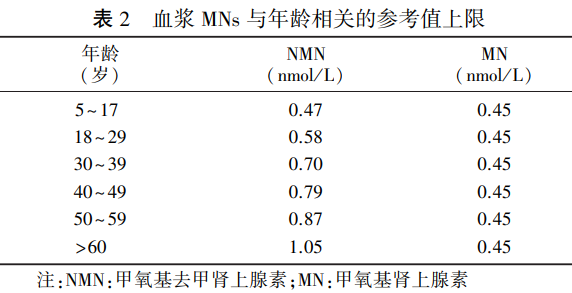
6. 药物干扰:三环类抗抑郁药、钙通道阻滞剂、拟交感神经药、单胺氧化酶抑制剂等可升高 CA 及 MNs 水平,如患者服这些药物则检测前应停用。 具体干扰测定的药物如下所示。
◆干扰 CA、MNs: 安定、阿替洛尔、拉贝洛尔、麻黄碱、伪麻黄碱、哌唑嗪。
◆干扰 NE、NMN: 阿米替林、米帕明、咖啡酸、3,4- 二羟扁桃酸、酚苄明、可可碱、L - 酪氨酸。
◆干扰 MNs: 苯丙胺、L - 苯丙氨酸、肼苯达嗪、5 - 羟基苯乙酸、血清素、茶碱。
◆干扰 NE: 硝苯地平、α- 甲基 NE。
◆干扰 CA: 咖啡因、西米替丁、3,4 - 亚甲基二氧基安非他明、尼古丁。
◆干扰 NMN: 对乙酰氨基酚、甲基多巴。
◆干扰 DA: 卡比多巴、 L - 多巴、组氨酸、α- 甲基 DA、章鱼胺。
◆干扰 3-MT:3,4 - 二羟苯乙酸、脱氧肾上腺素。
7. 正常参考区间: (1) 国外报道正常参考值上限:血浆游离 NMN 浓度 0.6 ~ 0.9 nmol/L、MN 浓度 0.3~0.6 nmol/L;其诊断 PPGL 灵敏度为 89.5% ~100%; 特异度为 79.4% ~97.6%。 尿 NMN 3.0~3.8 μmol/L,尿 MN 1.2~1.9 μmol/L;其灵敏度为 85.7% ~ 97.1%,特异度为 68.6% ~95.1%。 美国梅奥诊所实验室 LC-MS/MS 检测正常坐位血浆游离 MN<0.50 nmol/L、游离 NMN< 0.90 nmol/L 。 (2) 上海瑞金医院报道,当血浆游离 NMN 浓度为 0.8 nmol/L 时,诊断 PPGL 的灵敏度和特异度分别为 95% 和 90%;血浆游离 MN 浓度在 0.4 nmol/L 时诊断的灵敏度和特异度分别为 51% 和 90% 。
# (二) CA 水平测定
建议:采用 LC-MS/MS 或 HPLC-ECD 测定血或尿 NE、E 和 DA 浓度以帮助诊断 PPGL (2 | ●●●○)
1. 24 h 尿 CA 水平:当检测血或尿 MNs 水平不能完全除外 PPGL 时,测定 CA 则有助于确诊。 目前,国内外关于 CA 及代谢物的测定还没有实现检测标准化,检测结果在不同实验室还存在很大差异,故应该先建立各个实验室的检测正常参考区间。
正常人尿 CA 排泄量呈昼夜周期性变化,在活动时排泄量增多。 尿 CA (NE+E) 正常排泄量为 591 ~ 890 nmol/d (100 ~150 mg/d),其中 80% 为 NE,20% 为 E。 大多数 PPGL 患者尿 CA 均明显增高;少数阵发性高血压患者,不发作时尿 CA 水平可正常。
北京协和医院用 HPLC-ECD 测定 24 h 尿 CA 的正常参考范围为 NE (28.67 ± 11.98) mg/d (16.69 ~ 40.65 μg/d),E (4.08 ± 2.34) mg/d (1.74 ~ 6.42 mg/d),DA (225.76 ± 104.83) mg/d (120.93 ~ 330.59 μg/d) 。
北京解放军总医院采用 HPLC-ECD 检测 24 h 尿 CA 正常参考值范围为 NE 22.1 ~ 75.3 μg/d,尿 E 1.5 ~ 34.5 μg/d,尿 DA 93.2~470.3 μg/d 。
2. 血浆 CA 浓度测定:患者空腹、卧位休息 30 min 后抽血,正常人在平卧及安静状态时血浆 NE 浓度 <500 ~ 600 pg/ml ( 3.0 ~ 3.5 nmol/L), E 浓度 < 100 pg/ml (545 pmol/L);大多数 PPGL 患者血浆 NE>1 500 pg/ml (9 nmol/L),E>300 pg/ml (1.6 nmol/L) 。
美国梅奥诊所实验室用 HPLC-ECD 测定血浆 NE 正常参考区间为卧位 70 ~ 750 pg/ml,立位 200 ~ 1 700 pg/ml;E 卧位≤111 pg/ml,立位≤141 pg/ml;DA 30 pg/ml 亦无体位变化。
3. 对 CA 测定结果有干扰的药物:如利尿剂、肾上腺 α- 及 β- 受体阻滞剂、扩血管药、钙通道阻滞剂等,外源性拟交感药物及甲基多巴、左旋多巴可导致假阳性结果,故检测前应停用。 血浆 CA 测定结果可受环境、 活动等因素影响,应激状态和焦虑患者的血浆 CA 水平亦可升高。
# (三) CA 其他代谢产物测定
VMA 是 NE 及 E 的最终代谢产物,24 h 尿中的正常值 <7 mg/d ( 35 mmol/d); 诊断 PPGL 灵敏度为 46% ~77%,特异度为 86% ~ 99%,但应同时检测血、尿 CA 和 MNs 水平。
HVA 是 DA 的最终降解产物,正常值 <7 mg/d (45 nmol/d),神经母细胞瘤筛查诊断检测的主要代谢产物为 HVA 和 VMA。
3-MT 是 DA 的中间代谢产物,检测 3-MT 可提高筛查头颈部 PGL 的灵敏度; PPGL 患者血浆 DA 及 3-MT 浓度明显增高则高度提示为转移性肿瘤。
(四) CA 及代谢产物检测结果的诊断意义
测定血浆或尿液中 CA 及中间代谢产物、最终代谢产物浓度对 PPGL 定性诊断的灵敏度和特异度不同,其中 MNs 的灵敏度和特异度优于 CA 和 VMA。 因肿瘤可阵发性分泌释放 NE 和 E 并被多种酶水解,故测定 NE 和 E 水平可为正常,但 MNs 水平可升高,因此检测 MNs 可明显提高 PPGL 的诊断灵敏度。
采用 CA 水平诊断 PPGL 的灵敏度为 69% ~ 92%, 特异度为 72% ~ 96%;尿 CA 和 VMA 的诊断阳性率分别为 76% 和 88%。 假阴性率:MNs 为 < 5%,CA 为 1%~ 21%,VMA 为 10%~29%。
测定血浆游离或尿 MNs 水平诊断 PPGL 的灵敏度高,但假阳性率 19% ~ 21%。 血浆 MNs 灵敏度和特异度优于尿液 MNs;尿游离 MNs 诊断性能优于尿分馏 MNs;卧位血浆 MNs 假阳性率低于坐位 MNs。 如果以 NMN 或 MN 单项升高 3 倍以上或两者均升高做判断标准则假阳性率降低,但临床应进一步检查以进行确诊;对 MNs 轻度升高的患者应排除影响因素后进行重复测定。
同时测定血及 24 h 尿 CA 和 MNs 水平有较高的灵敏度和特异度,当疑诊患者血浆或尿 CA 和 MNs 水平高于正常参考值上限 1.5 ~ 2 倍时可提示 PPGL 诊断;但如仅稍高于正常参考值上限则应多次复查并做进一步检查以帮助诊断。 如能同时或多次测定基础状态下及高血压发作时的血或尿 CA 及 MNs 浓度,则可进一步提高 PPGL 的诊断符合率,如多次尿 CA 高于正常上限者应高度怀疑 PCC 可能。
二、 其他辅助测定
1. 嗜铬粒蛋白 A (chromogranin A, CGA):CGA 是一种酸性可溶性单体蛋白质,伴随 NE 在交感神经末梢颗粒中合成、储存及释放,PPGL 患者的 CGA 水平增高,其诊断灵敏度为 83%,特异度为 96%。
2. 神经元特异度烯醇化酶 (NSE): 非转移性 PPGL 患者的血浆 NSE 水平正常,约半数转移性 PPGL 患者明显增高,故测定血浆 NSE 水平可用于鉴别转移性 / 非转移性肿瘤。
3. 肾素、血管紧张素、醛固酮水平测定:PPGL 患者因 CA 分泌增多和血容量减少,可激活肾素 - 血管紧张素 - 醛固酮系统 (RAAS) 而致继发性醛固酮分泌增多,有的患者可伴有低钾血症,故测定肾素、血管紧张素、醛固酮水平可帮助判断患者血容量水平。
4. 药理激发或抑制试验:因药理试验的灵敏度和特异度差,并有潜在风险,故不推荐使用。
# 影像学定位诊断
当确定 PPGL 的定性诊断后应及时进行肿瘤的定位检查,以决定有益有效的治疗方式。
# 一、 CT 及三维重建
推荐:首选 CT 作为 PPGL 肿瘤定位的影像学检查 (1 | ●●●○)。
CT 为无创性检查,对胸、腹和盆腔组织有很好的空间分辨率,并可发现肺部转移病灶,目前已广泛应用于临床。
PPGL 瘤体在 CT 片上显示为密度不均匀的圆形或类圆形软组织影,肿瘤内常有坏死、出血或钙化,瘤体可被造影剂增强;转移性 PPGL 瘤体较大、密度不均、外形不规则、可有周围组织浸润或远处非嗜铬组织转移;如瘤体较小可有假阴性。 三维 (冠、矢状位) 重建及血管显像 (CTA) 可清楚显示肿瘤形态、供血及与周围组织的关系。 增强 CT 诊断 PPGL 的灵敏度为 85% ~98%,特异度为 70%。
# 二、 MRI
推荐:MRI 用于以下情况 (1 | ●●●○)。
1. 探查颅底和颈部 PGL。
2. 已有肿瘤转移的患者。
3. 体内存留金属异物伪影。
4. 对 CT 显影剂过敏。
5. 儿童、孕妇、已知种系突变和最近有过度辐射而需要减少放射性暴露的人群。 MRI 定位诊断 PPGL 的灵敏度为 85% ~ 100%,特异度为 67%。
# 三、 分子功能影像学
(一) 131I-MIBG 闪烁扫描
建议:有转移或不能手术的 PPGL 患者先进行131I-MIBG (国外用123I-MIBG) 核素显像,根据肿瘤的功能和解剖定位来评价131I-MIBG 治疗的可能性 (2 | ●●●○)。
MIBG 是肾上腺能神经阻断剂,与 NE 结构类似, 可被肿瘤组织的小囊泡摄取并储存,用放射性131I 标记 MIBG (131I-MIBG) 是第一个用于诊断和治疗 PPGL 的分子影像技术。 患者静脉注射131I-MIBG 后 24、48 h 进行融合显像, 如为高分泌功能的肿瘤则表现为131I-MIBG 显影阳性。 目前,在国内131I-MIBG 显像是发现肾上腺外 PGL 的功能定性和解剖定位的重要检查方法, 其灵敏度为 78% ~ 83%, 特异度为 100%, 当131I-MIBG 为肿瘤阳性显影时则可确定 PPGL 诊断。 不能手术治疗的转移性 PPGL 患者,如131I-MIBG 显影阳性则可进行131I-MIBG 治疗。
国外目前采用空间和时间对比度更高、检测微小病灶更敏感的 123 I 标记 MIBG 显像,其诊断 PPGL 灵敏度高于 131 I-MIBG, 123 I-MIBG 诊断 PCC 的灵敏度为 85% ~88%、特异度为 70% ~100%;诊断 PGL 的灵敏度为 56% ~ 75%、特异度为 84% ~ 100%。 但目前国内无此药。
MIBG 显像对转移性、复发性、位于颅底、颈部、胸腔、膀胱的 PGL 和与 SDH 各亚型 (尤其是 SDHB) 基因相关 PPGL 检出的灵敏度较低;对低分泌功能、较小肿瘤的显影效果较差,可出现假阴性。
拟交感神经药、阻断 CA 转运药物如可卡因和三环类抗抑郁药、钙通道阻滞剂、α- 及 β- 肾上腺素能受体阻滞剂等可减少 123 I-MIBG 浓聚,故需停药 2 周后再行 MIBG 显像;显像前 3 天应服用 Lugol 碘溶液以保护及避免甲状腺对 131 I 的摄取。
(二) 生长抑素受体显像 ( somatostatin receptor scintigraphy)
建议:用生长抑素受体显像筛查转移性 PGL 病灶 (2 | ●○○○)。
部分 PPGL 肿瘤有生长抑素受体高表达,故标记的生长抑素类似物可用于高灵敏度的 PPGL 分子影像学诊断。 99m Tc-OCT - 单光子发射计算机断层成像 (SPECT;生长抑素奥曲肽显像) 可对 131 I-MIBG 显影阴性的 PPGL 进行互补检查而帮助确诊。 对头颈部 PGL 肿瘤定位的灵敏度为 89% ~ 100%,明显优于 MIBG (18% ~ 50%);对 PGL 定位的灵敏度 (80% ~ 96%) 高于 PCC (50% ~60%)。
(三) 其他分子影像学检查
PPGL 分子影像学近年进展很快,CA 类似物如 11C - 羟基麻黄碱 (HED), 18 F - 氟苄基胍 (MFBG) 和 18 F- 多巴以及 CA 前体 18 F - 二羟基苯丙氨酸 (FDOPA) 均被用于标记正电子发射计算机断层扫描 ( PET/CT) 显像。 18 F 放出的正电子湮灭后发射光子而成像,故图像质量高,能准确定位,灵敏度和特异度均很高,转移性肿瘤的检出率也高,临床上可根据患者基因类型、肿瘤性质、部位、激素分泌等选择个体化的检查。
1. 建议:选择 18 氟 - 多巴 PET/ CT 用于肾上腺外的交感性 PGL、多发性、转移性和 (或) SDHB 相关突变的 PPGL 的定位诊断 (2|●●●○)。 其显像效果好,对转移性 PPGL 的诊断灵敏度为 88%,但价格昂贵。
2. 建议:选择 18 氟 - 脱氧葡萄糖 (18 F-FDG) PET/ CT 用于单个和转移的 PPGL 定位诊断 ( 2 | ● ● ○○)。 PPGL 患者因低氧改变而导致糖酵解代谢增加,恶性肿瘤因生长代谢快,需大量摄取葡萄糖而表现为放射性摄取增高的阳性病灶,故可根据标准摄取值 (SUV) 升高的程度即最大标准摄取值 (SUVmax) 来判断转移性 PPGL 肿瘤的可能性。 18 F-FDG 对非转移性 PPGL 的诊断灵敏度为 77%、 特异度为 90%, 与 123 I-MIBG 的灵敏度 (75%) 和特异度 (92%) 相近,但在转移性 PPGL 患者中 18 F-FDG 的灵敏度 ( 83%) 高于 123 I-MIBG (50%)。
3. 建议:选择 68Ga-Dotatate 标记的生长抑素类似物用于 PPGL 的分子影像学诊断 (2 | ● ● ○○)。 PPGL 肿瘤高度表达生长抑素受体, 68Ga-Dotatate PET/ CT 对 PCC 和 PGL 诊断灵敏度分别为 97.4% 和 95.8%, 其肿瘤检出率明显高于 CT/MRI、 18 F - 多巴、 18 F-FDOPA 和 18 F-FDG;如显影阳性也提示可应用 177 Lu-Dotatate 类似物进行转移性 PPGL 肽类受体核素治疗的可能性 (表 3)。 总之,PPGL 定位诊断较困难,常规 CT、MRI 解剖形态定位检查不易发现肾上腺外 PGL 肿瘤; 131 I-MIBG 可同时进行 PPGL 形态和功能定位,其特异度高但灵敏度较差,有时可为假阴性; 131 I-MIBG 显像阴性时可做生长抑素 ( 奥曲肽) X 线透射性计算机断层 (TCT) 与放射性核素发射式计算机断层 (ECT) 融合显像有助确诊; 68Ga-Dotatate PET/CT 并不是所有 PPGL 的首选显像;其他分子影像学的发展提供了新的靶向定位检查;因此,应根据患者的病情进行个体化选择 (图 1)。
# 遗传学及表观遗传学检测
# 一、 基因检测
推荐:所有 PPGL 患者均应到有条件的正规实验室进行基因检测,对所有转移性 PPGL 患者应检测 SDHB 基因 (1 | ●●●○)。 建议:根据肿瘤定位、性质和 CA 生化表型选择不同类型的基因检测 (2 | ●● ●○);对有 PPGL 阳性家族史和遗传综合征表现的患者可直接检测相应的致病基因突变 (2 | ●●●○; 图 2)。
PPGL 的发生与致病基因突变有关,目前已知有 20 多个致病基因,每年也不断发现新的基因。 约 50% 的 PPGL 患者有基因突变,其中 35% ~ 40% 为胚系突变,15% ~25% 为肿瘤体系突变;50 ~ 70% 的儿童 PPGL 与基因胚系突变有关。
PPGL 相关的基因突变涉及到细胞内不同信号转导通路,可分为与缺氧通路有关的 C1 型 (Cluster 1): 通过激活低氧诱导因子 (HIF),促进与缺氧有关的生长因子表达,从而刺激肿瘤生长,包括与低氧、假性低氧和与三羧酸循环通路相关的基因如 VHL、SDH 各亚型、HIF2A、延胡索酸水化酶 ( FH) 、脯氨酸羟化酶 (PHD) 1、PHD2、苹果酸脱氢酶 (MDH) 2 等。 C2 型 (Cluster 2): 通过激活丝裂原活化蛋白激酶 (MAPK)、 雷帕霉素靶蛋白 (mTOR) 的丝氨酸 / 苏氨酸蛋白激酶信号转导通路和蛋白质翻译激活的基因促进肿瘤生长,如 RET、 RAS、 NF1、 MAX 等基因和跨膜蛋白 TMEM127、核组蛋白 H3F3A 等致病因子。
VHL、RET、NF1、TMEM127 或 MAX 基因突变常见于 PCC 患者,且多为双侧肾上腺受累;RET 基因突变见于 MEN 2 型患者;SDHB 和 FH 基因突变提示为转移性 PGL。 有 RET 和 NF1 基因突变的 PCC 主要分泌 E,而 VHL、 SDH 亚型突变的 PPGL 则分泌 NE。 有 SDH 各亚型基因突变的患者多发生头颈部及交感神经性 PGL (表 1)。
上海瑞金医院在 563 例中国汉族 PPGL 患者中发现胚系基因突变 111 例 (19.7%), 其中 RET 50 例 (8.9%), VHL 25 例 ( 4.4%), SDHB 19 例 ( 3.4%), SDHAF2 5 例,SDHA 4 例,SDHD、MAX、TMEM127 各 2 例,NF1 和 SDHC 各 1 例。
2017 年美国国立卫生研究院 (NIH) 的人类基因组学研究 —— 癌症基因组图谱 ( The Cancer Genome Atlas, TCGA) 显示 69% PPGL 患者的基因胚系突变率 27% ( SDHB 9%、RET 6%、VHL 4%、NF1 3%, SDHD、 MAX、PHD2 和 TMEM127 突变率均 < 2%);体细胞突变率 39%;融合基因 7% (其 5% 为 MAML3 融合基因)。 89% PPGL 患者有 DNA 拷贝数变异 (SDHB 57%、VHL 36%、SDHD 23%、TP53 34%、NF1 24%)。 根据 TCGA 研究及 mRNA 表达特点又将 PPGL 分成激酶信号 (kinase signaling)、假性低氧 ( pseudohypoxia)、Wnt 改变 (Wnt-altered) 和皮质混合 (cortical admixture) 这 4 个亚型。
在肿瘤组织中行 SDH 亚型基因的免疫组织化学染色可帮助检测 PPGL 患者是否有 SDH 亚型胚系突变,如 SDHB 染色阴性的 PPGL 患者术后密切随访,应除外转移性肿瘤的可能。
# 二、 表观遗传学
PPGL 组织中多种基因存在异常高甲基化,包括抑癌基因、DNA 修复基因、细胞周期调控、肿瘤转移相关基因等。 由于肿瘤组织普遍存在基因组的低甲基化和启动子区 CpG 岛的高甲基化,引起原癌基因及促进细胞生长的基因激活,抑癌基因及错配修复基因失活及染色体不稳定。 PPGL 肿瘤 DNA 甲基化和 miRNA 表观遗传学研究可为转移性肿瘤的早期诊断及治疗靶点提供依据。
# 治疗
PPGL 是涉及到多学科的内分泌复杂疑难性疾病,由内分泌科或高血压门诊进行初始诊治,组建多学科团队分工协作,进行分阶段协同诊治非常重要。
# 一、 手术治疗
PPGL 的定性、定位诊断明确后应尽早手术切除肿瘤,非转移性 PPGL 经切除肿瘤可得到治愈;转移性 PPGL 如能被早期发现,及时手术也可延缓生命。 近年来经腹腔镜行肾上腺肿瘤微创切除术取得了良好疗效并已广泛应用,极大地减少了手术创伤和并发症,减轻患者痛苦,缩短住院天数及降低医疗费用。
因 PPGL 是功能性肿瘤,术前应做好充分的药物治疗准备,避免麻醉和术中、术后出现血压大幅度波动或因致命的高血压危象发作、肿瘤切除后出现顽固性低血压而危及生命,做好充分的术前准备是降低手术死亡率的关键。
推荐:除头颈部副交感神经性 PGL 和分泌 DA 的 PPGL 外,其余患者应先用 α- 受体阻滞剂做术前准备 (1 | ●●●○)。 推荐:术后 24 ~ 48 h 要密切监测患者的血压和心率 (1 | ●●○○)。
# (一) 术前准备原则
可用选择性 α1 - 受体阻滞剂或非选择性 α- 受体阻滞剂控制血压,如治疗后血压未能控制,再加用钙通道阻滞剂。 使用 α- 受体阻滞剂后,如患者发生心动过速,则加用 β- 受体阻滞剂。 绝对不能在未用 α- 受体阻滞剂之前先用 β- 受体阻滞剂,以免发生急性心功能不全。 α- 甲基酪氨酸抑制 CA 合成,可与 α- 受体阻滞剂短期联合使用控制血压,并减少围手术期血流动力学波动 (目前国内无此药)。 此外,患者应摄入高钠饮食和增加液体摄入,补充血容量,防止肿瘤切除后引起严重低血压。
# (二) 常用治疗药物
1. α- 肾上腺素能受体阻滞剂。
◆ 酚妥拉明 (通用名 phentolamine, 商品名 Regitine,下同) : 是一种短效、非选择性 α- 受体阻滞剂,对 α1 和 α2 两种受体的阻断作用相等,其作用迅速,半寿期短,故需反复多次静脉注射或持续静脉滴注。 常用于高血压诊断试验 (Regitine 试验) 、治疗高血压危象或在手术中控制血压,但不适于长期治疗。
◆酚苄明 (phenoxybenzaming, Dibenzyline): 是非选择性 α- 受体阻滞剂,对 α1 受体的阻断作用较 α2 受体要强近百倍,口服后吸收缓慢,半寿期 12 h,作用时间长,控制血压较平稳,常用于手术前药物准备。 初始剂量 5 ~ 10 mg,每日 2 次,视血压控制情况逐渐加量, 可每 2 ~ 3 d 增加 10 ~ 20 mg,平均剂量 0.5 ~ 1 mg・kg-1·d-1 ,大多数患者需服 40 ~ 80 mg/d 才可控制血压,少数患者需要更大剂量,术前至少服药 2 周以上。 不良反应有心动过速、体位性低血压、鼻黏膜充血致鼻塞等,故应监测卧、立位血压和心率变化,嘱咐患者起立动作要慢,以防摔倒。
◆哌唑嗪 (prazosin, Minipress)、特拉唑嗪 (terazosin, Hytrin)、多沙唑嗪 (doxazosin, Cardura): 均为选择性突触后 α1 - 受体阻滞剂,不影响 α2 受体。 在服用首次剂量后易发生严重体位性低血压,应嘱患者卧床休息避免摔倒,必要时逐渐加量。
多沙唑嗪初始剂量 2 mg/d,终剂量 32 mg/d。
◆乌拉地尔 (urapidil, Ebrantil): 也是非选择性 α- 受体阻滞剂,可阻断突触后 α1 - 受体及外周 α2 受体, 但以前者为主。 还可激活中枢 5 - 羟色胺 - 1A 受体,降低延髓心血管调节中枢的交感反馈作用,因此在降压时对心率无明显影响。 PPGL 高血压危象时可用静脉输液泵入,根据血压水平调整剂量。
2. β- 肾上腺素能受体阻滞剂。
用 α- 受体阻滞剂后,β- 肾上腺素能相对增强可致心动过速、心肌收缩力增强、心肌耗氧量增加。 β- 肾上腺素能受体阻滞剂可阻断心肌 β 受体,降低肾上腺能兴奋性而使心率减慢,心搏出量减少,血压下降。
◆普萘洛尔 (propranolol): 非选择性 β- 肾上腺素能受体阻滞剂,可阻断心脏 β1 受体及支气管、血管平滑肌 β2 受体,初始剂量 10 mg,2 ~ 3 次 /d,逐渐增加剂量以控制心率。
◆阿替洛尔 (atenolol): 选择性 β1 - 肾上腺素能受体阻滞剂,因无明显抑制心肌收缩力的作用,故优于普萘洛尔。 初始剂量 25 mg,1 次 /d,终剂量 50 mg/d。
◆美托洛尔 (metoprolol): 选择性 β1 - 肾上腺素能受体阻滞剂,可减慢心率,减少心输出量,初始剂量 12.5 mg,2 次 /d,终剂量 25 mg,2 次 /d。
◆艾司洛尔 (esmolol,Brevibloc): 短效的选择性 β1 - 肾上腺素能受体阻滞剂,作用快而短暂,半寿期为 9 min,可用于静脉滴注,迅速减慢心率。
# (三) 术前准备充分的标准
1. 持续性高血压血压≤140/90 mmHg,阵发性高血压发作频率减少、幅度降低。
2. 血容量恢复:红细胞压积降低,体重增加,肢端温暖,无明显体位性低血压。
3. 高代谢症群及糖代谢异常改善。
4. 术前药物准备时间存在个体差异,一般为 2 ~ 4 周,伴严重并发症的患者,术前准备时间应相应延长。
# (四) 术中血压监测及管理
1. 手术中持续监测血压、心率、中心静脉压、心电图、肺动脉楔压等。
2. 术中出现血压升高,可静脉滴注或持续泵入酚妥拉明或硝普。
3. 如心率显著加快或发生快速型心律失常,可在使用 α- 受体阻断剂后,静脉用速效 β1 - 受体阻滞剂艾司洛尔治疗。
# (五) 补充血容量
切除肿瘤后如患者血压下降或出现低血压,立即停用 α- 受体阻滞剂,并快速补充血容量,维持中心静脉压正常,必要时使用血管活性药物。
# (六) 手术
推荐:对大多数 PCC 行腹腔镜微创手术,对肿瘤直径 > 6 cm 或者侵袭性 PPGL 进行开放式手术以确保完整切除肿瘤,术中防止肿瘤破裂,并避免局部复发或种植复发 (1 | ●●○●)。 推荐:对 PGL 行开放式手术 (1|●●○○);对小肿瘤、非侵袭性 PGL 也可行腹腔镜手术 (2|●○○○);双侧 PCC 应采取保留皮质的肾上腺切除术,以免发生永久性肾上腺皮质功能减退 (2 | ●●○○)。
# 二、 术后监测
推荐:术后 24 ~ 48 h 密切监测患者的血压和心率 (1 | ●●○○)。
1. 术后注意以下患者发生继发性肾上腺皮质功能 减退的可能性:(1) 双侧肾上腺部分切除;(2) 孤立肾 上腺的单侧肾上腺部分切除。
2. 术后 2~4 周复查生化指标以明确是否成功切除肿瘤。
# 三、 转移性 PPGL 的治疗
转移性 PPGL 的治疗是较大的难题,也是进展比较快的领域,目前已经开展和正在进行临床试验的有下述治疗。
(一)131I-MIBG 治疗
1. 治疗适应证: 131I-MIBG 核素显像阳性、无法手术的患者。
2. 治疗剂量:国内常用 200 mCi / 次,2~3 次 / 年,累计治疗剂量 800~1 000 mCi。
3. 肿瘤疗效评估:每次治疗后至少半年内应行检查评估,包括血压、血象、肝肾功能、血 / 尿 CA 及 MNs、 影像学等。 治疗完全有效率 3% ~ 5%,部分有效率和病情稳定率可达 73% ~79%,患者的 5 年生存率增加, 达 45% ~68%。
4. 不良反应:最常见骨髓抑制 (包括中性粒细胞和血小板减少),也有骨髓增生异常综合征、急性或慢性髓系白血病的报道。
2018 年美国食品药品监督管理局 (FDA) 以孤儿药资格批准了超痕量 iobenguane 131I (注册名 Azedra ®) 治疗无法手术或化疗以及治疗后进展的转移性 PPGL 患者,超痕量131I-MIBG 具有较高放射性比度 (放射性物质的放射性活度与其质量之比) ,更易进入转移性 PPGL 肿瘤中,故疗效佳,68% 的患者治疗后肿瘤病情稳定、耐受性良好、不良反应更少。 但目前国内暂无此药。 2019 年美国国家综合癌症网络 ( National Comprehensive Cancer Network,NCCN) 已将131 I-MIBG 治疗转移性 PPGL 列入临床肿瘤指南。
(二) 177Lu-Dotatate
部分 PPGL 肿瘤能高度表达生长抑素受体,肽类受体介导的放射性核素治疗 (peptide radioreceptor therapy, PRRT) 是一种用于治疗转移性神经内分泌肿瘤患者的新技术。 目前,正在进行的177Lu-Dotatate 治疗转移性 PPGL 的 Ⅱ 期临床试验为68Ga-Dotatate 标记的生长抑素受体显像阳性的 PPGL 患者提供了新的核素治疗方法。
(三) 抗肿瘤药物联合化疗
1. CVD 方案:即环磷酰胺 (cyclophosphamide)、长春新碱 (vincristine) 和达卡巴嗪 ( dacarbazine),CVD 方案多在 2~4 个疗程后起效,治疗完全有效率、部分有效率及病情稳定率分别为 4%、37% 和 14%。 不良反应主要有骨髓抑制、血白细胞减少、周围神经病变、神经系统毒性、胃肠道反应、肝功能异常和低血压等;治疗中也可能出现高血压危象。
2. 替莫唑胺和沙立度胺联合应用:治疗已转移的神经内分泌肿瘤具有较好疗效,2 年生存率 61%。
3. 依托泊苷 (etoposide) 和顺铂 ( cisplatin),即 EP 方案。
(四) 酪氨酸激酶抑制剂靶向治疗
舒尼替尼是一种酪氨酸激酶抑制剂、卡博替尼是强效抗血管生成的酪氨酸激酶抑制剂、帕唑帕尼是靶向作用于血管内皮生长因子受体、血小板衍生生长因子受体和纤维母细胞生长因子受体的一种多种酪氨酸激酶抑制剂、阿西替尼是一种高选择性的酪氨酸激酶抑制剂,目前都正在做临床试验观察。
(五) 细胞程序性死亡蛋白受体 1 (PD-1) 抗体
有些肿瘤通过激活 PD-1 而逃避免疫系统攻击, 目前一项使用 Pembrolizumab 治疗转移性 PPGL 的 Ⅱ 期临床试验正在进行中。
(六) 奥曲肽 (Octreotide) 或兰瑞肽 (Lanreotide)
2019 NCCN 临床实践指南推荐用于治疗生长抑素受体显像阳性、肿瘤未能切除、有远处转移的 PPGL 患者,可用奥曲肽 150~ 250 mcg 皮下注射 (3 次 /d) 或奥曲肽微球制剂 20 ~ 30 mg 肌肉注射或兰瑞肽 90 ~ 120 mg (两者均为每 4 周皮下注射 1 次)。
(七) 其他治疗
对肿瘤及转移病灶的局部放疗、伽马刀、射频消融和栓塞治疗等,可减轻患者的部分临床症状和肿瘤负荷,但对患者生存时间的改变却不明显。
# 预后及随访
手术成功切除肿瘤后,大多数 PPGL 患者的高血压可以被治愈,一般术后 1 周内 CA 恢复正常,75% 的患者在 1 个月内血压恢复正常,25% 的患者血压仍持续增高,但较术前降低,用一般降压药物可获得满意疗效。
非转移性 PPGL 患者手术后 5 年存活率 > 95%,复发率 < 10%;转移性 PPGL 患者 5 年存活率 < 50%。
PPGL 患者需终身随访,推荐每年至少复查 1 次; 有基因突变、转移性 PPGL 患者应 3 ~ 6 个月随访 1 次, 对其直系亲属应检测基因和定期检查 (1|●●●○)。
PPGL 是涉及到多学科的复杂疑难性疾病, 应组织多学科团队协同诊治。 实行 PPGL 患者个体化管理,每年至少复查 1 次;儿童、青少年、有 PPGL 家族史和有基因突变、转移性患者则应 3 ~ 6 个月随访 1 次, 包括症状、体征、血压、血 / 尿 MNs、CA 等检测,定期复查影像学检查;评估肿瘤有无复发、转移或发生 MEN 或其他遗传性综合征,对其直系亲属检测基因和定期检查
# PPGL 的诊断治疗流程
PPGL 的定性定位诊断和治疗,推荐按照以下流程图进行 (图 3)。
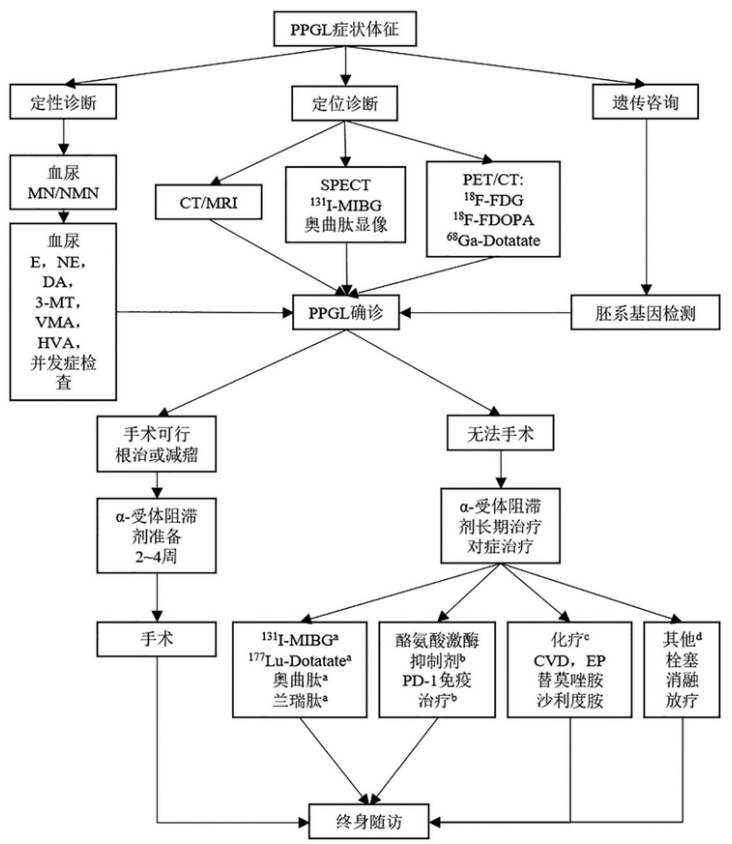
注:PPGL:嗜铬细胞瘤和副神经节瘤;MN:甲氧基肾上腺素;NMN:甲氧基去甲肾上腺素;E:肾上腺素;NE:去甲肾上腺素;DA:多巴胺;3-MT:3 - 甲氧基酪胺;VMA:香草扁桃酸;HVA:高香草酸;CT:计算机断层扫描;MRI:磁共振成像;SPECT:单光子发射计算机断层成像;131I-MIBG: 131碘 - 间碘苄基胍;PET/CT:正电子发射计算机断层扫描;18F-FDG:18氟 - 氟脱氧葡萄糖;68Ga-Dotatate:68镓 - 1,4,7,10 - 四氮杂环十二烷 - 1,4,7,10 - 四羧酸 - D 苯丙氨酸 I - 酪氨酸 3 - 苏氨酸 8 - 奥曲肽;SDH:琥珀酸脱氢酶;177Lu-Dotatate:Lutetium-177-DOTA°-Tyr3奥曲肽;PD-1:细胞程序性死亡蛋白受体 1;CVD:环磷酰胺 (cyclophosphamide) 长春新碱 (vincristine) 和达卡巴嗪 (dacarbazine) 方案;EP:依托泊苷 (etoposide) 和顺铂 (cisplatin) 方案;a:美国国家综合癌症网络 (NCCN) 2019 指南推荐;b:目前在做药物试验观察;c:疗效因人而异;d:观察疗效,因人而异
图 3 PPGL 的诊断治疗流程。
