 缺氧性肺血管收缩
缺氧性肺血管收缩
# 缺氧性肺血管收缩
Dunham-Snary KJ, Wu D, Sykes EA, et al. Hypoxic Pulmonary Vasoconstriction: From Molecular Mechanisms to Medicine. Chest. 2017;151(1):181-192. doi:10.1016/j.chest.2016.09.001
# 摘要
缺氧性肺血管收缩 (HPV) 是肺血管系统固有的动态平衡机制。肺内动脉收缩对肺泡缺氧的反应,将血液转移到氧合更好的肺段,从而优化通气 / 灌流匹配和全身氧气输送。作为对肺泡缺氧的响应,线粒体传感器动态地改变了肺动脉平滑肌细胞 (PASMC) 中的活性氧物种和氧化还原对。这抑制钾通道,去极化 PASMC,激活电压门控钙通道,并增加胞浆钙,引起血管收缩。持续低氧激活 Rho 激酶,加强血管收缩,激活低氧诱导因子 (HIF)-1a,导致不利的肺血管重构和肺动脉高压 (PH)。在未通气的胎儿肺中,HPV 将血液转移到全身血管系统。出生后,HPV 通常作为局灶性肺炎或肺不张的局部稳态反应发生,在不改变肺动脉压 (PAP) 的情况下优化全身 PO2。在单肺麻醉中,HPV 减少了流向不通气的肺的血液,从而促进了胸部手术。在高海拔地区,全身缺氧导致弥漫性 HPV,增加 PAP,并引发 PH。过高的或异质性的 HPV 导致高原肺水肿。相反,HPV 受损,无论是由于疾病 (如 COPD、败血症) 还是血管扩张剂药物,都会促进全身性低氧血症。这种氧感应通路的遗传和表观遗传异常可以触发氧正常状态下 HIF-1α 的激活,并可以促进异常代谢和细胞增殖。由此产生的假性低氧状态是 Warburg 代谢转变的基础,并有助于 PH 的肿瘤样表型。HPV 和氧感受器对人类健康和疾病都很重要。
# 序言
缺氧性肺血管收缩 (HPV) 最初由 Bradford 和 Dean1 发现,随后由 von Euler 和 Liljestrand2 鉴定。HPV 反映肺内小动脉对肺泡低氧的反应。3 HPV 可以是全局性的 (对环境低氧的反应),在这种情况下,肺动脉压 (PAP) 升高;然而,在大多数情况下,HPV 是由局灶性肺不张或肺炎引起的,肺泡缺氧和血管收缩都局限于一个肺段或肺叶。在这种情况下,血液从缺氧的肺段转移到肺的氧合较好的部分,而不会升高 PAP。结合胸部 X 线片和放射性同位素通气 / 灌注 (V/Q) 扫描,匹配的 V/Q 由肺部疾病引起的病变和 HPV (图 1A) 与不匹配的 V/Q 由肺栓塞引起的病变很容易区分 (图 1B)。
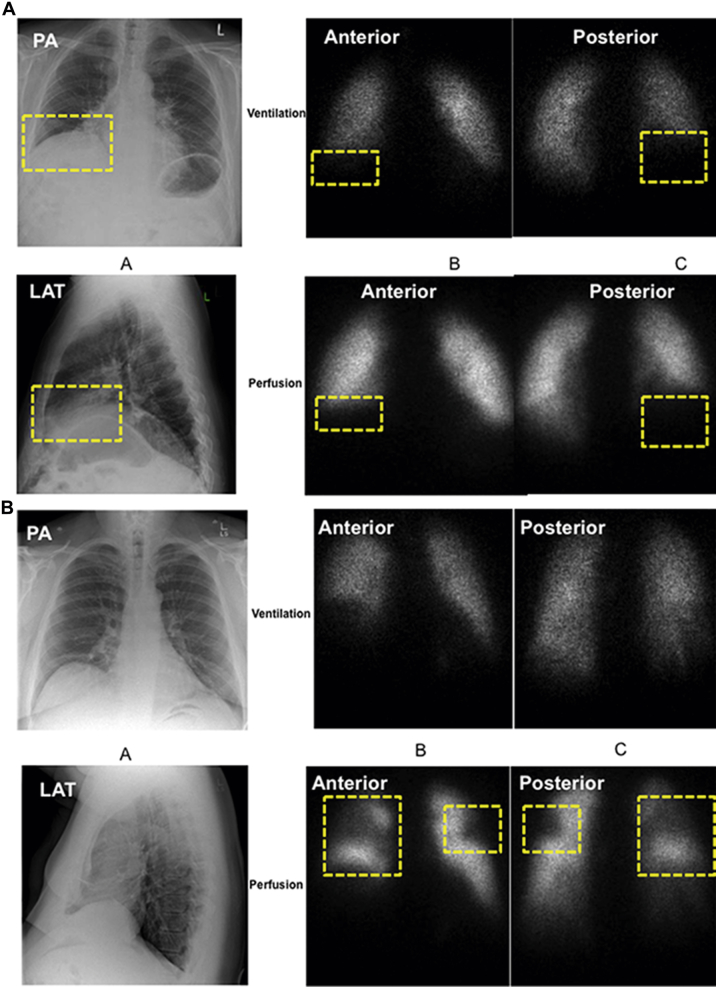
图 1. 通气 / 灌流 (V/Q) 匹配与失调的病变。(A) 因间质性肺疾病造成通气 / 灌流 (匹配的病变。一位 83 岁的老人因劳累而呼吸急促。胸部 CT 显示间质性肺疾病,基底部与常见的间质性肺炎高度一致。(B) 通气 / 灌流失调的病变,图示肺栓塞。一位 57 岁的男性,肥胖、高血压和阻塞性睡眠呼吸暂停综合症,表现为呼吸急促,轻微运动导致血氧饱和度下降。PA = 后前侧;LAT = 侧方。
# HPV 机制
HPV 的传感器和效应器机制一直是大量研究的主题。11、12、13、14、15 假设 HPV 的传感器机制驻留在线粒体中。16 经典公认的线粒体的功能是产生能量 (三磷酸腺苷 [ATP])。电子供体烟酰胺腺嘌呤二核苷酸 (NADH) 和黄素腺嘌呤二核苷酸 (FADH2) 的电子传递沿电子传递链 (ETC) 进行。ETC 组分之间的电子流量是由冠部脂溶性半喹酮调节的。当电子沿着氧化还原梯度流向末端电子受体 (分子氧) 时,质子就会穿过线粒体内膜。根据米切尔的化学渗透理论,17 跨膜的氢离子的聚集产生了电化学梯度,为 H + 转运体 F1FO 三磷酸腺苷酶复合体提供动力,并促进 ATP 的合成。
线粒体是原核生物内的共生体,在真核细胞内进化以支持多细胞生物体的能量需求。19 人们越来越认识到,它们具有许多非规范功能,包括氧气感受。20 线粒体形成由分裂、融合和易位形成的动态网络。线粒体网络的活细胞成像类似于建筑物中的电线 (图 2,视频 1)。不同于固定组织制备中的静态二维电子显微镜图像,使这些细胞器看起来是孤立的,在活的肺动脉平滑肌细胞 (PASMC) 中使用线粒体靶向荧光团显示,线粒体形成一个普遍的动态网络,到达细胞的所有区域,并动态地接触其他细胞器,如肌浆网。对线粒体形态的了解有助于理解传感器的功能。
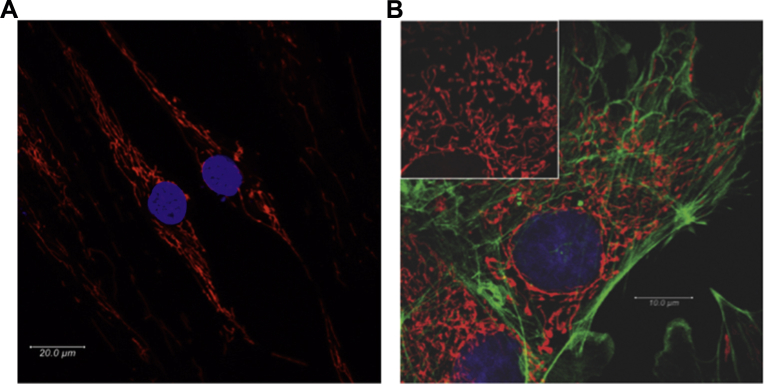
图 2. 肺动脉 (PA) 线粒体网络。(A) 用 20 nM 的四甲基罗丹明对正常患者的肺动脉平滑肌细胞线粒体进行染色,并用共聚焦显微镜进行成像。细胞核用 NucBlue 活细胞染色。(B) 牛肺动脉 (PA) 内皮细胞线粒体 (插图:红色,MitoTracker Red CMXRos)、鬼臼蛋白 (绿色,Alexa Fluor 488) 和细胞核 (蓝色,4‘,6 - 二氨基 - 2 - 苯吲哚) 染色,并用共聚焦显微镜成像。来自生命科技公司 (加利福尼亚州卡尔斯巴德) 的所有染料 / 污渍。
线粒体的感应器功能是生理电子流量的副产品,如图 3 所示。简而言之,在电子转移过程中,一些未耦合的电子产生活性氧物种 (ROS),特别是超氧化物,它被超氧化物歧化酶 2 (SOD2) 迅速转化为过氧化氢,过氧化氢是一种可扩散的氧化还原介体,调节氧化还原敏感离子通道和酶的活性,并充当信号分子。21,22 从目的上讲,氧传感器依赖于与 PO2 相连的参数 (即,ROS 的产生是电子通量的副产品),但位于 ATP 合成附近,允许对反缺氧的动态平衡反应,而不会有生物能量妥协的风险。哺乳动物体内稳态氧感应系统中的氧感应依赖于线粒体和其他氧化还原感受器控制的氧化还原化学。
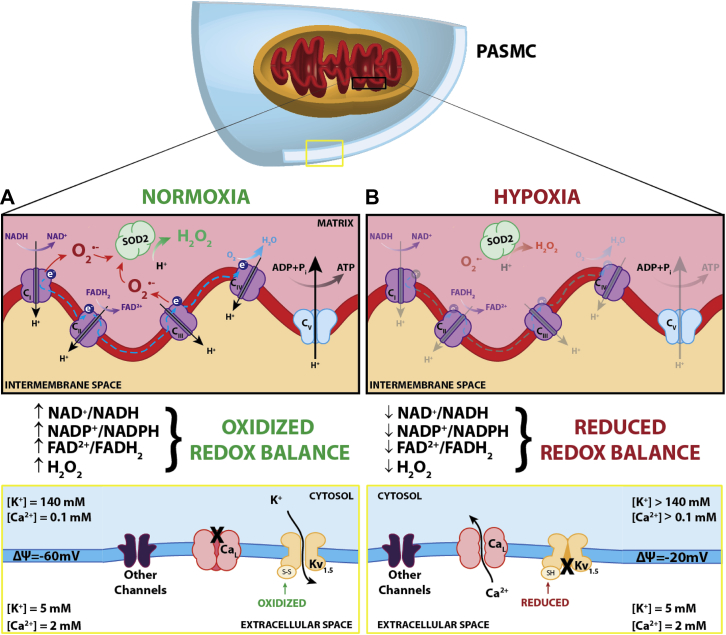
图 3. 线粒体氧化还原氧气感应。缺氧性肺血管收缩 (HPV) 的感应器效应机制。(A) 在常氧条件下,线粒体电子传递链 (ETC) 复合体 I 和 III 产生活性氧 (ROS),产生超氧化物 (O2-),超氧化物歧化酶 2 (SOD2) 将超氧化物歧化酶 2 (SOD2) 转化为过氧化氢 (H2O2)。过氧化氢与氧化的氧化还原对 (如烟酰胺腺嘌呤二核苷酸 [NAD+]、烟酰胺腺嘌呤二核苷酸磷酸 [NADP+] 和黄素腺嘌呤二核苷酸 [FAD2+]) 一起维持 Kv1.5 巯基氧化和通道开放状态,导致 K + 紧张性外流。这种 K + 外流维持细胞静息膜电位 (ΔΨ) 为 - 60 mV,并抑制电压门控钙通道 [Cal] 介导的钙内流。(B) 在缺氧期间,有限的氧气 (1) 防止过氧化氢的产生,(2) 降低氧化 / 还原对的比例,(3) 减少 Kv1.5 通道上的巯基,使它们关闭。随后 K + 的积聚使细胞的静息膜电位增加到 - 20 mV。这刺激了钙离子的开放,钙离子的内流,以及随后的收缩装置的激活 (即血管收缩)。ADP = 腺苷二磷酸;FADH2 = 黄素腺嘌呤二核苷酸;NADH = 烟酰胺腺嘌呤二核苷酸。
虽然 HPV 可被内皮衍生的血管收缩药 (如内皮素和血栓素) 升高,但可被内皮衍生的血管扩张药 (如一氧化氮和前列环素) 抑制,但其核心效应机制存在于 PASMC 内。这里,HPV 是由线粒体氧化还原信号触发的,该信号涉及电压和氧化还原敏感的钾和钙通道的协调反应 (图 3)。简单地说,电压门控性钾通道 (Kv) 维持约 - 60 mV 的静息膜电位 (反映了钾离子从 PASMC 的紧张性外流)。这种负膜电位降低了电压门控的 L 型钙通道的开放程度。外向钾电流在缺氧时受到抑制,使膜去极化,增加钙通道的开放概率,导致细胞内钙离子以 20,000:1 的细胞外 / 细胞内钙梯度流入细胞内。这种胞浆钙的升高和随后的 Rho 激酶介导的钙敏化导致 PA 收缩。
药理和电生理实验采用膜片钳技术研究 HPV.25,26,4 - 氨基吡啶对 Kv 和大电导电压门控钙通道 (Cal) 的抑制作用。Cal 通道阻滞剂硝苯地平和异搏定可抑制 HPV 的收缩反应,而钙通道激动剂 Bay K8644 可增强对 HPV 的收缩反应。然而,HPV 的这些效应成分在肺动脉和体动脉之间并没有本质上的区别,这两种动脉都对 K + 通道抑制剂有收缩反应,对钙通道阻滞剂有松弛反应。相反,对低氧反应的组织异质性主要是由于肺动脉和体动脉中的平滑肌细胞在氧感受器 (线粒体) 功能上的差异。
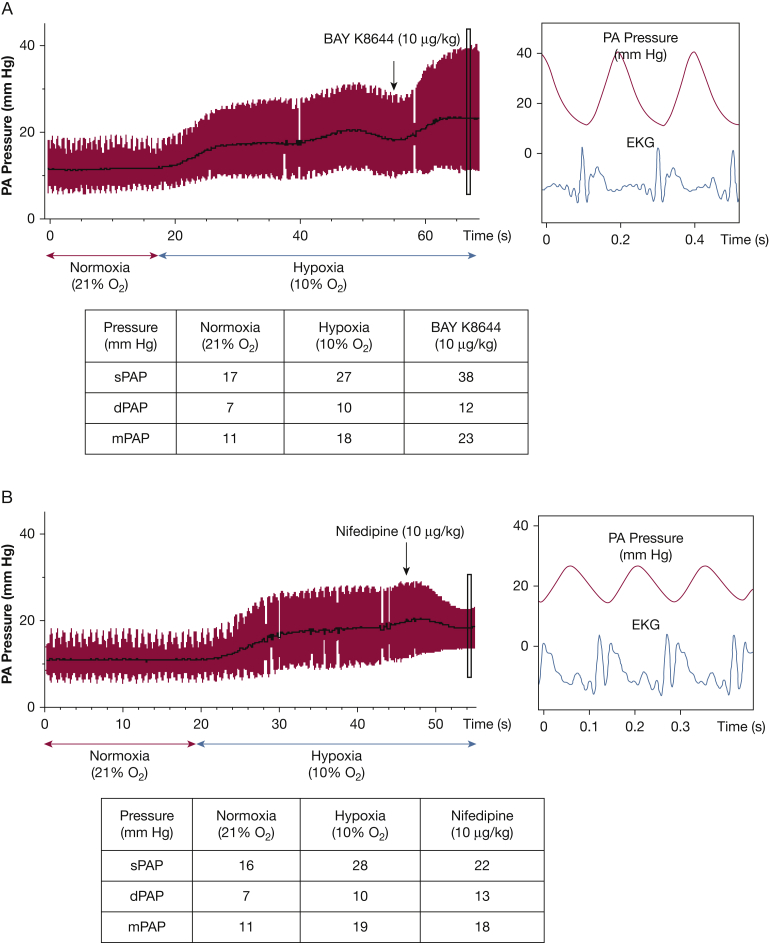
图 4. 电压门控钙通道与缺氧性肺血管收缩 (HPV)。Cal 激动剂 Bay K8644 和拮抗剂硝苯地平对 10% 氧气诱导的麻醉低氧大鼠 HPV 有相反的抑制作用。这种全球缺氧模型模拟了随着海拔的升高而发生的变化,并导致肺动脉压 (PAP) 的快速增加。(A) 在低氧时,Bay K8644 可增强 PA 的血管收缩作用。(B) HPV 期间应用硝苯地平可抑制 CAL,降低 PAP。DPAP = 舒张期 PAP;ECG = 心电图;mPAP = 平均 PAP;SpAP = 收缩 PAP。
对 HPV 涉及的离子通道的分子鉴定揭示了 Kv1.5 的中心作用,Kv1.5 是一种振荡器通道,Kv2.1.29,30 例如 Kv1.5 基因敲除小鼠,显著降低了 HPV 31。然而,有证据表明其他类别的 K + 和 Ca~(2+) 通道参与了 HPV 的发病机制,32 包括两孔 K + 通道,33,34,它们在非常负的膜电位下活跃,因此是 HPV 启动的有吸引力的靶点。尽管对这些通道的药物抑制不会导致肺血管收缩,34 其中一些可能与 PASMC 对低氧的电生理反应有关。同样,除了 L 型钙离子通道外,与 HPV 有关的钙离子也来源于钙离子诱导的钙离子释放。人乳头瘤病毒也反映了钙的敏感性。
尽管人们一致认为线粒体作为氧感受器,ETC 衍生的 ROS 改变了介导血管收缩的效应机制,但关于缺氧是否会导致 ROS / 过氧化氢水平的上升或下降仍存在争议。32、39、40、41、42、43 简要地说,有人提出低氧增加 ROS 并反映由于 ETC 的远端抑制而导致的 ETC 自氧化。41、42 相反,我们的发现表明,PASMC 中 ROS 的产生随着 PO2 的上升而增加,随着 PO2 的下降而下降。例如,我们观察到动脉导管平滑肌细胞出生时 ROS 水平随着 PO2 的增加而上升。44,45 同样,心肌细胞在缺血期间 ROS 水平较低,在心肌缺血 / 再灌注损伤的再灌注期,ROS 水平随着复氧而增加。46 我们观察到 PASMC 线粒体在生理性低氧期间 ROS (包括过氧化氢) 减少,反映了由于末端电子受体 (分子氧) 可获得性降低而导致的电子通量降低的速率。
那些发现缺氧是高 ROS41,42 的氧化状态与那些发现它是低 ROS23,43 的还原状态的人之间的差异的基础尚不清楚。实验差异可能与以下方面的差异有关:(1) 从阻力动脉中新分离的 PASMC 的使用,(2) 所用低氧的严重程度,(3) 对 pH 和 PCO2 的关注,以及 (4) 在亚细胞隔室动态和准确的 ROS 测量方面的挑战。支持缺氧是一种还原 (而不是氧化) 状态的观点,缺氧对 PA 与全身血管张力和细胞电生理的相反影响是由 ETC 抑制剂 (如鱼藤酮和抗霉素 A) 和还原剂 (如二硫苏糖醇) 模拟的,而不是由 ROS 和氧化剂模拟的。9、47 提出的机制应根据它们解释 HPV 核心属性的程度来判断,HPV 是快速、可逆的,由轻度缺氧引起,不会引起水肿。此外,一个统一的机制应该解释低氧对肺循环 (收缩) 和动脉导管和全身血管系统 (血管扩张) 的相反影响。
# HPV 临床意义
虽然 HPV 在正常人体生理和常见肺部疾病患者中很活跃,但临床医生对它的认识仍然不足。除了优化匹配和全身氧气输送外,HPV 还被用来通过外科手术来增强氧合。
对于接受胸部手术 (如肺肿瘤切除) 的患者,HPV 对单肺麻醉至关重要。48 在这些手术中,患者侧卧以便于手术解剖,并使用双腔支气管内管启动单肺通气 (图 5A)。在导管放置过程中,近端和远端管腔尖端分别位于隆突上方和靶肺的主支气管内 (图 5B)。每个管腔周围的袖带被充气,以防止空气泄漏,并允许非手术肺的选择性通风和手术肺的塌陷 (图 5C)。非通气肺内的 HPV 通过最大限度地减少分流而减少灌注量,否则会导致术中全身低氧血症 (图 5D) 和术野出血过多 (图 5E)。
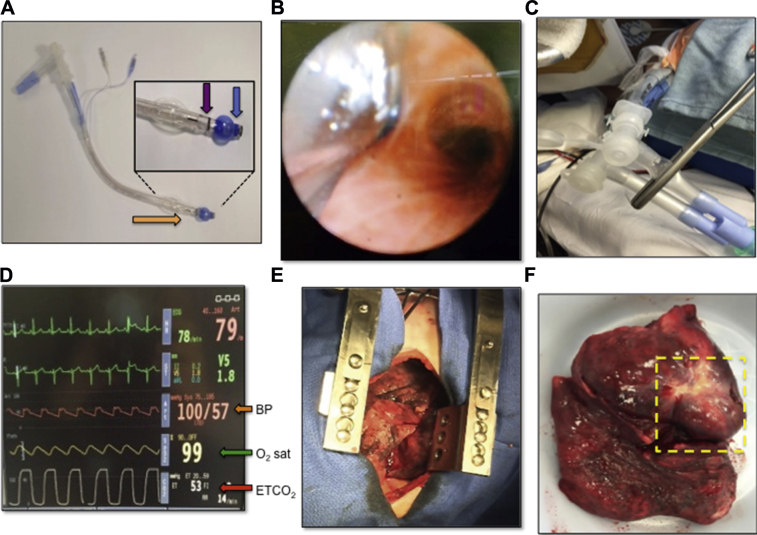
图 5. 低氧性肺血管收缩 (HPV) 的临床应用。单肺通气法维持开胸手术期间血氧饱和度的研究。(A) Broncho-Cath 双腔气管导管 (Covidien,Saint-Laurent,QC)。远端 (橙色箭头) 插入气管,直到支气管腔 (插图,蓝色箭头) 进入右或左主干支气管,而气管腔 (插图,紫色箭头) 保持在隆突上方。(B) 从气管管腔内的支气管镜下观察隆突。可以看到双腔气管导管的远端进入左主支气管处,以实现单肺通气。(C) 在通气回路的一端放置一个夹子,以允许对侧肺进行选择性通风。(D) 单肺麻醉 / 呼吸机期间的心肺监测。由于通气量减少,呼气末二氧化碳上升至 53 毫米汞柱 (红色箭头),而氧饱和度 (O2) 保持在 99%(绿色箭头),血压 (BP) 保持稳定 (橙色箭头)。(E) 手术中未通气的肺可通过切口处看到。由于 HPV 的反应,在手术中可以看到最少的出血。(F) 全肺切除标本,显示切除的完整肺和一个大的肿瘤 (黄色方框)。
HPV 在胸部手术中的益处可能会因药物或患者生理原因而减弱。挥发性麻醉剂、血管扩张剂和低温可以抑制 HPV。因此,可以调整麻醉药物的选择和温度,以优化单肺通气患者的 HPV。从历史上看,HPV 一直使用低剂量的呼吸兴奋剂阿米特林来增强药理作用。在单肺通气期间,在吸入的一氧化氮 (NO) 中加入阿米特林 (4μg/kg/min) 可增加人乳头瘤病毒并改善全身氧合。49 尽管阿米特林因可能导致周围神经病变而退出临床使用,但该药物说明了增强人乳头瘤病毒作为改善匹配和全身氧合的手段的价值。
HPV 还通过减少不匹配和分流来优化肺不张、肺炎、COPD 和哮喘患者的全身 PO2 (表 1)。在肺炎或肺不张期间,HPV 通过减少低氧段的灌流来优化全身氧气输送。HPV 在肺不张缓解 (例如,拔除粘液塞子或使用激励性肺活量测定法) 或肺炎消退时迅速逆转。HPV 的强度因个体而异,可随疾病或药物治疗而减弱 (表 1)。例如,钙通道阻滞剂通常用于全身高血压或冠状动脉疾病 (COPD 的并存),可降低 HPV。服用硝苯地平 (20 毫克) 的肺心病 (COPD 继发的肺动脉高压) 患者的动脉血氧分压 (PO2) 从 52 毫米汞柱下降到 47 毫米汞,并伴随着匹配的恶化。65 给药途径决定了 PA 血管扩张剂对 HPV 的影响。吸入性血管扩张剂 (如吸入 NO) 可能会增强匹配性,因为它们只到达通风良好的肺段 (因此不会损害 HPV);相反,静脉注射血管扩张剂通过松弛为通风不良的肺段提供的小动脉来恶化匹配。66 例如,在造成兔肺隔离灌流模型 PH 后,Walmrath 等人 66 证明,尽管静脉注射前列环素血管扩张剂可降低平均肺动脉压 (MPAP)(从 35 mm Hg 降至 25 mm Hg),但它也使分流分数增加 (至约 60%)。相比之下,吸入 NO 同样会降低 mPAP,但将分流分数维持在约 25%。66
表 1 呼吸疾病中 HPV 的作用
| 疾病 | HPV 的作用 | 处置 | 参考文献 |
|---|---|---|---|
| HAPE | HPV 过强;未收缩的肺血管过度灌流 | 钙通道阻滞剂硝苯地平将 HAPE 的发生率从 63% 降低到 10% | 50 (opens new window), 51 (opens new window), 52 (opens new window), 53 (opens new window) |
| Asthma | HPV 在急性支气管收缩期间保持 V/Q 平衡 | 静脉注射异丙肾上腺素可降低哮喘大鼠肺灌流模型的 mPAP (降低 3-5 毫米汞柱) | 53 (opens new window), 54 (opens new window), 55 (opens new window), 56 (opens new window) |
| COPD | HPV 降低;然而,残留反应改善了 V/Q 平衡和全身氧合。 | 在 COPD 患者中,阿米特林 (100 mg/d),一种增强 HPV 的药物,使 PaO2 从 52 毫米汞增加到 59 毫米汞 | 53 (opens new window), 57 (opens new window), 58 (opens new window), 59 (opens new window) |
| Pneumonia | 将血流从病变肺叶分流出来优化全身血氧饱和度 | 肺炎在实验模型中损害 HPV;在 COPD 伴缺氧加重时,静脉注射前列腺素增加全身低氧血症,与抑制 HPV 的不良反应一致 | 53 (opens new window), 57 (opens new window), 60 (opens new window), 61 (opens new window), 62 (opens new window) |
| ALI/ARDS | ALI 中 HPV 减少;然而,残留的 HPV 改善 V/Q 平衡并减少分流 | 在 ARDS 的绵羊模型中,抑制诱导型一氧化氮合酶可恢复 HPV,增加 PaO2/FiO2,并减少分流分数 | 53 (opens new window), 57 (opens new window), 63 (opens new window), 64 (opens new window) |
ALI = acute lung injury; HAPE = high-altitude pulmonary edema; HPV = hypoxic pulmonary vasoconstriction; mPAP = mean pulmonary artery pressure; NOS = nitric oxide synthase; = ventilation/perfusion.
# 高原长期暴露对 HPV 的抑制作用
抑制 HPV 是一种常见的对高海拔生活的适应。原产于中亚喜马拉雅地区 (海拔> 3,500 米) 的牦牛 (Bos Grunniens) 使 HPV 变钝,因此维持低 PAP。67 相反,家牛 (Bos Taurus) 土生土长于低海拔地区,在海拔地区表现出大量的 HPV,导致约 20% 的牛出现严重的 PH、水肿和右心衰。由于奶牛的解剖结构,这种依赖性的水肿聚集在颈部 (胸廓区域),而不是像人类那样聚集在腿部。这种颈部肿胀使这种致命的 HPV 过度和右心衰竭综合征得名。69 原产于高海拔地区的牛不太容易出现夸大的 HPV 和胸肌疾病。67,70 牦牛和牛的杂交导致动物表现出中等 HPV。Anand 等人发现 DZO (牛和牦牛的杂交) 具有与牦牛相似的肺血流动力学。相比之下,DZO 与公牛杂交会产生一头公牛。其中一半的粪便具有与牦牛相似的肺血流动力学,而另一半则与奶牛相似。70,72 Newman 等人通过比较易感牛和耐药牛来评估夸大的 HPV 和高原 PH 的遗传学 (海拔地区的 PAP 分别为 86±13 mm Hg 和 35±1 mm Hg)。在高原敏感牛中,46 个基因表达上调,14 个基因表达自我调节。基因芯片分析发现,易感牛的呼吸道疾病和炎症性疾病途径紊乱。易感表型与异常白介素 6、触发髓系细胞上表达的受体、过氧化物酶体增殖物激活受体和核因子 κB 信号有关。68 全外显子测序表明 HIF-2α 编码基因 (内皮 PAS 结构域蛋白 1 [EPAS1]) 突变参与了牛高原 PH 的发病机制。在 75% 的 mPAP 升高的牛 (>50 mm Hg) 和所有研究的高海拔牛 (mPAP>94 mm Hg) 中,发现 EPAS1 的一个双变异体导致 HIF-2α 氧依赖降解区的两个非同义氨基酸替换。推测该双变异体是导致多种 HIF-2α 靶点上调的功能突变,如血管内皮生长因子和转化生长因子 -α.73
人群在海拔高度也表现出 PAP 的遗传变异。经过数千年的海拔高度 > 4000 米的生活,本土藏族人表现出最小的缺氧 PH(HPH)或红细胞增多症。74 相比之下,HPH 在居住在厄瓜多尔和玻利维亚安第斯高地的魁丘亚印第安人中普遍存在,海拔约 3500 至 4000 米.71,75 同样,科罗拉多州铅维尔(北美最高城市约 3100 米)的儿童也是如此。通常展示 HPH。Leadville 居民的 HPH 严重程度与 Quechua 相似,尽管 Coloradans 的海拔高度要低得多。Grover70 表明,Leadville 的许多健康运动儿童表现出 HPH(mPAP,静息和运动时分别为 28 mm Hg 和 61 mm Hg)。这表明近期高海拔居民人群中度无症状 PH 的患病率较高。因此,假设 HPV 和 HPH 的大小与高海拔地区的进化持续时间成反比(藏族人 25000 年,安第斯魁北克省约 13000 年,科罗拉多州人口不到一个世纪)。这些在人类和动物群体中的研究表明易感性或对慢性缺氧的抗性的遗传传递,并且这些变化可能与氧传感途径组分的表达和功能的变化有关。
# HPV 过度并急性暴露于高原可导致高原肺水肿
如果不适当适应氧气压力的降低而迅速上升到高海拔地区,可能会导致高原肺水肿(HAPE),这是一种非心源性肺水肿,其特征是咳嗽,呼吸困难和运动能力下降,通常在提升至海拔 > 2500 米的 2 至 5 天内发病 [76]。夸大的异质性 HPV 与 HAPE51,52 的病理生理学有关(表 1)。PAP 迅速上升应力并扩张动脉壁。在短时间内,这些变化超过了阻力 PA 的负荷能力,导致基底膜和肺泡 - 毛细血管屏障破裂 [77]。有趣的是,HAPE 表现出个体易感性,最常见于夸大 HPV 的人群。夸大 HPV 的 10% 白人对 HAPE 特别敏感。Dehnert 等 [78] 评估了 421 名天真到高海拔的健康白人;受试者暴露于常压缺氧(模拟 4500 m) ,并使用多普勒超声心动图测量 PAP。39 名受试者在模拟上升到 4559 m 超过 24 小时(缺氧时收缩期 PAP,516 毫米汞柱)。这些志愿者中有四名(13%)在 48 小时暴露期间经历了 HAPE。相反,没有 HPV 正常强度的受试者(缺氧时的收缩期 PAP,33±5 mm Hg)经历过 HAPE。此外,在升高到海拔高度的实验模型中,抑制 HPV 可降低 HAPE。用乙酰唑胺(33μM)(其是临床上用于预防 HAPE 的药剂)处理的分离的灌注兔肺显示出比对照肺(缺氧 mPAP 约 20mm Hg)更少的 HPV(缺氧 mPAP 约 15mm Hg)。79
除肺泡 - 毛细血管屏障破裂外,低氧还会抑制肺泡液在肺内的清除。在正常情况下,通过钠通道和交换器重新吸收钠会在肺内产生渗透梯度,从而允许重新吸收水分。低氧抑制钠交换器的活性,从而减少钠的转运,最终减少肺内液体的重吸收。
只要患者得到及时的适当治疗,HAPE 是可逆的。改善氧合是最终目标,通常是通过补充氧气和从海拔快速下降。患者通常在补充氧气和休息的治疗后几个小时内好转。在低海拔地区,临床症状有望在几天内完全恢复。80 在紧急情况下,当不能立即下降时,用抑制 HPV 的药物,如硝苯地平或西地那非,治疗 HAPE 可以缓解症状,直到可以安全地下降到较低海拔。
# 假性低氧与 Chuvash 病
另一例病理性 HPV 出现在 Chuvash 病中。Chuvash 病以俄罗斯伏尔加河中游地区命名,尽管氧气浓度正常,但 HPV、红细胞增多症和 PH 均有所增强。82 名 Chuvash 病患者在 von Hippel-Lindau 基因 (VHL) 内有错义突变。这种突变削弱了 VHL 与 HIF-1α 和 HIF-2α 的 α 亚基相互作用的能力。在常氧条件下,HIF 蛋白被脯氨酸羟基酶羟化,这导致它们被 VHL 泛素化,从而靶向 HIF 蛋白酶体的降解。在缺氧过程中,HIF 蛋白不会被羟化,也不会被 VHL 结合,因此降解会受到损害。Chuvash VHL 突变削弱了 VHL-HIF 相互作用的能力,导致常氧性 HIF 稳定和 HIF 调节基因的矛盾常氧性转录,如红细胞生成素。因此,Chuvash 病患者的功能就像他们由于正常氧感觉紊乱而暴露在慢性缺氧中。
与丘瓦什病的患者一样,小黄头鼠随着年龄的增长会自发地患上 PH 和轻度红细胞增多症。它们也有 HIF-1α 的常氧激活,尽管在小鹿头罩大鼠中这反映了线粒体 SOD2.85 的表观遗传沉默。HIF 也是一种氧化还原调节的氧敏感机制 86;然而,其蛋白质转录介导的效应比离子通道启动的血管对低氧的反应起效慢。氧感觉紊乱的情况提醒我们,假低氧信号可能导致人类疾病,如 HPH。事实上,癌症中的 Warburg 范式是氧感知受损导致新陈代谢、细胞增殖和细胞凋亡异常的另一个例子。
# 结论
PASMC 在小阻力 PAS 中能够感知氧的变化并触发 HPV,从而优化氧摄取和全身氧输送。HPV 反映了线粒体氧化还原传感器和效应器之间的优雅相互作用,效应器包括氧化还原敏感的离子通道、酶和转录因子。人乳头瘤病毒在胎儿循环中很重要,在优化正常人体的氧合方面也很活跃。HPV 可优化各种肺部疾病的全身氧气输送,包括肺不张、肺炎和慢性阻塞性肺病。临床医生应该注意,血管扩张剂药物无意中抑制 HPV 可能会导致错配和全身性低氧血症;相反,可以通过抑制 HPV 来预防或治疗 HAPE。人乳头瘤病毒也可以在单肺通气期间被利用,以促进肺部手术。
