 铜绿假单胞菌呼吸机相关性肺炎抗生素治疗8天与15天比较
铜绿假单胞菌呼吸机相关性肺炎抗生素治疗8天与15天比较
# 铜绿假单胞菌呼吸机相关性肺炎抗生素治疗 8 天与 15 天比较:一项随机、对照、开放标签试验
Bouglé A, Tuffet S, Federici L, et al.: Comparison of 8 versus 15 days of antibiotic therapy for Pseudomonas aeruginosa ventilator-associated pneumonia in adults: a randomized, controlled, open-label trial. Intensive Care Med 2022; 48:841–849
2022 年 6 月 21 日发表了一篇文章的 [更正]
本文已更新
# 摘要
# 目的
非发酵革兰阴性杆菌 (NF-GNB) 包括铜绿假单胞菌 (PA) 引起的呼吸机相关性肺炎 (VAP) 的抗生素疗程仍不确定。我们旨在评估短期抗生素治疗(8 天)相对于长期抗生素治疗(15 天)在 PA 引起的 VAP (PA-VAP) 中的非劣效性。
# 方法
我们进行了一项全国范围、随机、开放标签、多中心、非劣效性试验,以评价 PA-VAP 抗生素治疗的最佳疗程。符合条件的患者是确诊为 PA-VAP 的成人患者,并以 1:1 的比例随机分配接受短疗程(8 天)或长疗程(15 天)。采用预先规定的分析评估复合终点,即死亡率和 90 天内重症监护室 (ICU) 住院期间 PA-VAP 复发率的结合。
# 结果
研究在 24 个月后由于入选率缓慢而停止。在意向治疗人群 (n = 186) 中,15 天组发生复合终点事件的患者百分比为 25.5%(n = 25/98),8 天组为 35.2%(n = 31/88)(差异 9.7%,90% 置信区间 (CI)-1.9%-21.2%)。在 ICU 住院期间,15 天组和 8 天组的 PA-VAP 复发百分比分别为 9.2% 和 17%。
两组在 ICU 住院期间的机械通气中位天数、ICU 住院天数、肺外感染例数和获得性多药耐药 (MDR) 病原体例数相似。
# 结论
我们的研究未能显示短疗程抗生素治疗 PA-VAP 相对于长疗程的非劣效性。短疗程策略可能与 PA-VAP 复发增加相关。然而,缺乏效度限制了本研究的解释。
关键信息
目前尚不清楚铜绿假单胞菌呼吸机相关性肺炎的最佳疗程。在这项前瞻性随机试验中,我们没有证明短期(8 天)抗生素治疗的非劣效性。
# 引言
呼吸机相关性肺炎 (VAP) 仍是重症监护病房 (ICU) 发病和死亡的主要原因,占 ICU 患者感染的 25%。尽管有治疗 VAP 的指南框架 [1]、[2]、[3]],但仍存在一些不确定性,尤其是治疗铜绿假单胞菌 (PA-VAP)[[4]]。因此,抗生素治疗 PA-VAP 的最佳疗程仍有争议。少数研究报告了根据抗生素疗程的复发率 [[5]、[6]]。在 PneumA 试验 [5] 中比较了 VAP 使用抗生素 8 天与 15 天的治疗效果,如果说各组间支气管镜检查 28 天后的死亡率和肺炎复发率没有差异,那么非发酵革兰阴性杆菌 (NF-GNB) 引起的 VAP 患者(多数为铜绿假单胞菌)短疗程组的肺炎复发率就会高于长疗程组(40.6% 对比 25.4%)。但是,PneumA 的二次分析发现,抗生素使用时间对复发或死亡率没有影响 [7]。 值得注意的是,在最近的荟萃分析 [6] 中,虽然发现短疗程在死亡率(比值比 (OR) 1.18;95% 置信区间 (CI) 0.77-1.8)和肺炎复发率 (OR 1.41;95% CI 0.94-2.12) 方面具有非劣效性,但是在 NF-GNB 导致的 VAP 病例中,短疗程后的复发率更高(OR 2.18;95% CI 1.14-4.16),死亡风险无差异。即使是 NF-GNB VAP 北美或欧洲指南推荐的也是较短的疗程 [1],[2],[3]]。因此,PA-VAP 最佳治疗时间仍存在一些疑问,需要在前瞻性随机研究中解决。因此,在铜绿假单胞菌呼吸机相关性肺炎 (iDIAPASON) 患者研究中,抗生素疗程对临床事件的影响旨在评估抗生素短疗程(8 天)相比抗生素长疗程(15 天)在 PA-VAP 中的非劣效性。
# 方法
# 研究设计
这项全国、随机、开放标签、多中心、非劣效性、对照试验 (NCT02634411) 的设计之前已发表 [[8]]。简言之,我们连续筛选确诊为 PA-VAP 的成人(≥18 岁)。PA-VAP 的诊断包括临床怀疑 [1](≥2 项标准,包括发热 > 38.5 ℃、白细胞增多 > 109/L 或白细胞减少 < 4×108/L、脓性气管支气管分泌物、以及胸部 x 线检查发现新的或持续性浸润)和呼吸道样本定量培养铜绿假单胞菌阳性进一步确诊:支气管肺泡灌洗液(显著阳性 /mL)或定量气管内抽吸肺内分泌物样本(阳性阈值≥106 cfu/mL)。 如果出现以下情况,患者不符合入选标准:妊娠、免疫抑制(HIV、免疫抑制治疗、皮质类固醇 > 0.5 mg/kg/ 天且持续超过 1 个月)、目前具有治疗肺外感染的铜绿假单胞菌活性的抗生素治疗、撤除生命支持措施,铜绿假单胞菌的慢性肺部定植【在入住 ICU 前 6 个月内,慢性阻塞性肺病 (COPD) 或支气管扩张没有肺炎或没有急性加重的情况下获得的呼吸道标本,其阳性结果低于铜绿假单胞菌的阈值(即,受保护的样本刷 < 103 cfu/mL,支气管肺泡灌洗 < 104 cfu/mL 或气管吸出物 < 106 cfu/mL)】。本研究按照赫尔辛基宣言和法国法律法规进行。该研究已获得法国伦理委员会 (Comitéde Protection des Personnes Ile de France VI) 以及法国药品安全局 (Agence Nationale de Sécuritédu Médicament et des Produits de Santé) 的批准。根据法国法律 [9],在患者入选前或患者亲属或紧急入选时获取书面知情同意书。补充材料中描述了关于试验设计的其他详细信息,包括研究者职责。
# 试验干预
在细菌学呼吸道采样后立即开始抗生素治疗,不等待微生物学分析结果(细菌鉴定和 / 或抗生素敏感性试验结果)。 初始抗生素治疗的选择由医生根据临床情况、既往抗生素治疗、是否存在多重耐药 (MDR) 病原体的风险因素 [[1] 或之前 90 天内是否住院(当前住院≥5 天,机械通气≥5 天,在透析中心或养老院接受支持治疗),当地流行病学数据,最后一次已知患者携带的 MDR 病原体。在这些情况下,建议立即使用广谱抗生素,联合使用 β- 内酰胺 /β- 内酰胺酶抑制剂或抗假单胞菌头孢菌素和氨基糖苷类或抗假单胞菌氟喹诺酮 3-5 天。如果是早发性肺炎(机械通气 < 5 天)并且没有多重耐药病原体的风险因素,可以按照推荐 [[[1]、[2]、[3]]] 使用窄谱的初始抗生素治疗。强烈建议研究者根据培养结果和药敏试验将这一初始方案转化为更窄的抗菌谱治疗。根据随机分组,必须在第 8 天或第 15 天结束时停止抗生素治疗,除了抗生素治疗确诊的肺部感染复发或新发肺外感染。在 ICU 入院时,通过对直肠拭子样本中产超广谱 β- 内酰胺酶肠杆菌科细菌 (ESBL) 和前鼻孔拭子样本中耐甲氧西林金黄色葡萄球菌 (MRSA) 的监测培养进行 MDR 病原菌的筛选,然后每周一次直至 ICU 出院。
# 随机化
获得抗生素敏感性试验结果后,将患者按照区组平衡的 1:1 比例随机分配,并使用互联网 (CleanWEB,Telemedicine Technologies,S.a.S) 在 8 天组或 15 天组进行中心分层。研究者对区组大小保持盲态。
# 主要和次要结局
主要结局是综合 ICU 住院期间直至第 90 天发生的死亡率和 PA-VAP 复发的复合终点。复发的定义是由两名独立的专家根据预先规定的标准对治疗组设盲的事后诊断:对铜绿假单胞菌未进行有效抗生素治疗至少 48h 后临床疑似 VAP,定义为至少存在下列体征之一(发热 > 38.5 ℃,白细胞增多 > 109/L 或白细胞减少 < 4×108/L)伴脓性气管支气管分泌物,胸片显示新发或持续浸润,然后证实定量培养阳性,如上所述。如果两名专家 (C-EL、FB) 意见不一致,则由第三名专家 (CD-F) 达成共识。
在 ICU 停留直至第 90 天期间评价的次要结局是有创机械通气 (MV) 时间、ICU 住院时间、抗生素暴露时间、肺外感染的数量和类型以及获得性 MDR 病原体(来自直肠和前鼻孔的拭子样本)。
# 统计分析
根据欧洲药品管理局的指南 [[10],该研究旨在根据 10% 的非劣效性界值,证明 8 天策略相比 15 天策略在 90 天时的死亡率和复发率复合终点方面的非劣效性。 假设 15 天策略中 PA-VAP 的死亡率和 / 或复发率为 35.7%[[11]],10% 的非劣效性界值将在单侧 α 风险为 5% 的情况下达到 80% 的效度,考虑到 5% 的脱落率,目标需要 600 例随机分组的患者。
根据其分布,使用频率和百分比报告分类数据的基线特征,使用均值和标准差 (sd) 或中位数和四分位距 (IQR) 报告连续数据的基线特征。
分析的主要终点针对意向治疗 (ITT) 人群进行,定义为 “随机分组患者”。通过 CI 方法评估非劣效性(精确双侧 90%(1-2α) CI,相当于 α 值为 0.05 的单侧检验)。如果组间差异的 CI 上限低于 10%,则可以认为 8 天组非劣效于 15 天组。在符合方案 (PP) 人群中进行敏感性分析,PP 人群定义为随机分配的患者,排除错误纳入的患者或不遵守分配的抗生素疗程的患者(医学原因除外)。使用 Kaplan–Meier 生存曲线表示 ITT 人群的无事件生存期,考虑到 VAP 复发或从有效抗生素治疗到 90 天死亡的事件,使用 Cox 模型估计风险比 (HR) 及其 90% CI。在事后分析中,使用具有二项式分布和 logit 连接的广义线性混合模型计算 ITT 和 PP 人群中校正的组间比例差异及其双侧 90% CI,考虑中心作为随机效应,并校正了以下基线变量:心力衰竭、高血压、给予儿茶酚胺和 PaO2/FiO2 比值。比较组间 VAP 复发率的差异及其精确的 90% CI。 使用 Kaplan–Meier 生存曲线和 Cox 模型估计的 HR 及其 90% CI 表示从有效抗生素治疗到 ICU 死亡或到第 90 天删失的时间。作为事后分析,考虑到 Fine 和 Gray 模型的死亡竞争风险,进行了 VAP 无复发生存率分析。结果表示为亚分布风险比 (sHR) 及其 90% CI,并绘制累积发生率曲线。采用贝叶斯方法和 β- 二项式模型进行事后敏感性分析 [12]。
在优效性假设下分析次要结局。使用组间差异及其精确 95% CI 比较 ICU 住院期间 MDR 病原体的获得率。使用组间中位数差异及其 95% CI(Mood 方法)比较有创机械侵通气、ICU 住院时间、抗生素暴露和 ICU 住院期间肺外感染的数量。
未替换主要结局的缺失数据,因为无数据缺失。在事后分析中,PaO2/FiO2 比值的缺失数据用每组的中位值替代。除了 CI 中位差异估计采用 R Studio 版本 1.2.5019 (R:A Language and Environment for Statistical Computing,R Core Team,R Foundation for Statistical Computing,Vienna,Austria,[https://www.R-project.org]),采用 STATA 软件第 17 版 (StataCorp,USA) 进行的敏感性校正分析,使用 R 版本 4.1.1 (2021-08-10) 的 —“Kick Things”【版权 (C) 2021 The RFoundation for Statistical Computing,Platform:x86_64-apple-darwin 17.0 (64-bit)】进行 Bayesian 分析,其他所有分析均采用 SAS 软件 9.4 版(SAS Institute Inc.Cary,NC,USA)。
# 资金来源的作用
申办方为 Assistance Publique-Hôpitaux de Paris(Département de la Recherche Clinique et du Développement,临床研究和开发部)。 该研究由 program Hospitalier de Recherche Clinique—PHRC 2014 (Ministère de la Santé) 的基金资助。
# 结果
# 患者
2016 年 6 月 3 日至 2018 年 5 月 22 日期间,30 家中心于 2016 年 6 月至 2018 年 5 月招募了 196 例患者,其中 190 例接受了随机化。24 个月后由于入选率缓慢而停止研究。事实上,估计需要 6 年才能入组 600 例患者,以证明复合终点的非劣效性。2 例患者拒绝参加,2 例患者处于监护中,结果 186 例患者进行了 ITT 分析。在排除 34 例严重偏离方案者(患者错误入组 (n = 32) 和随机化不符合 (n = 2))的患者后,PP 人群纳入了 152 例患者([1]). 错误入选的原因详见补充文件 1。在总体人群中,患者大部分为男性 (75.8%),年龄为 59.4±17.4 岁,有高血压病史 (25.3%)。入住 ICU 时首次诊断为急性循环衰竭 41 例 (22%)、急性呼吸衰竭 35 例 (18.8%)、创伤 35 例 (18.8%)。表 1 中报告了基线特征。
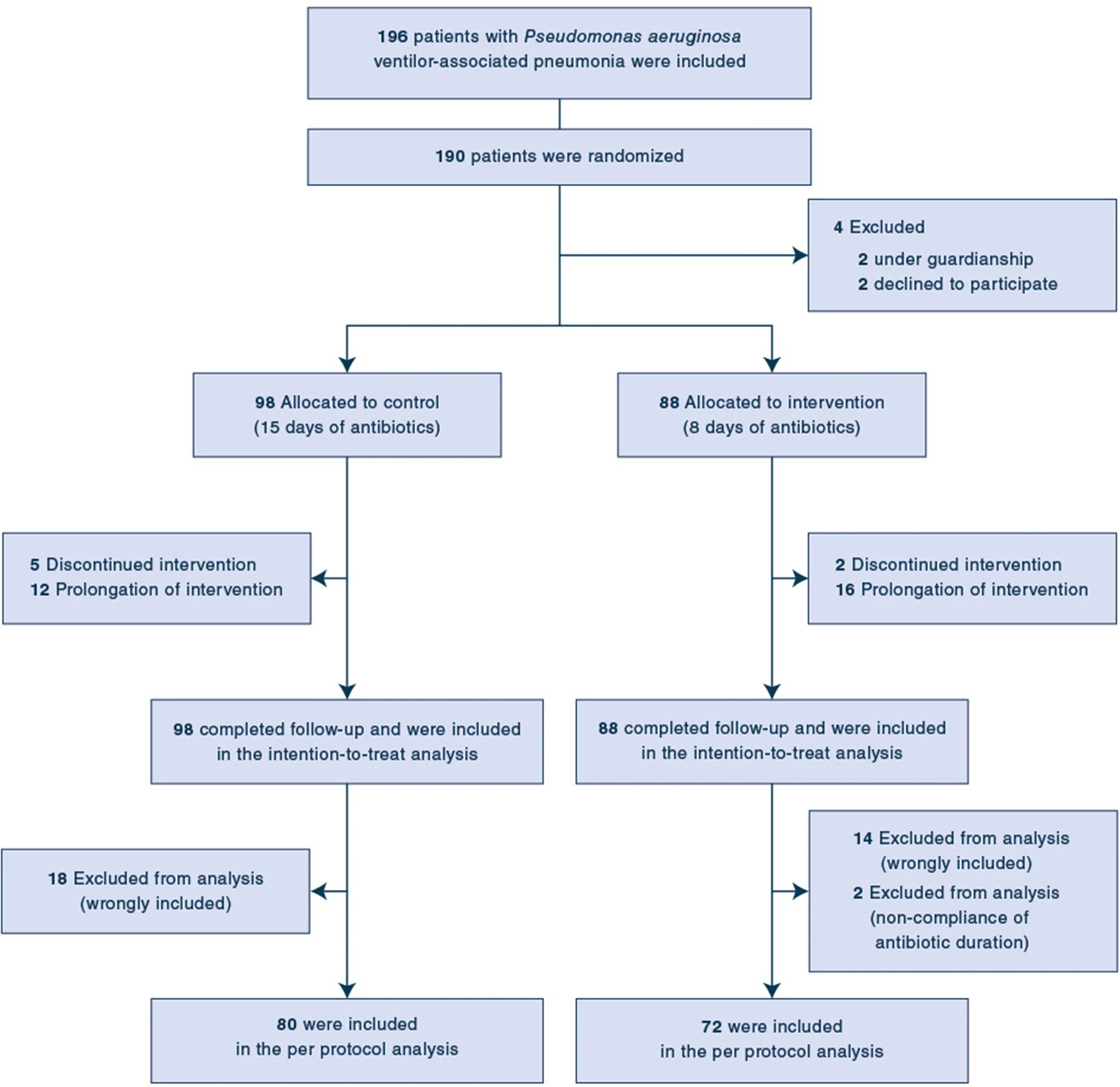
图 1 研究流程图
表 1 意向治疗人群的基线特征
| 15 天组 (N = 98) | 8 天组 (N = 88) | |
|---|---|---|
| 人口统计学特征 | ||
| 年龄 - 岁,m±sd | 59.2 ± 18.3 | 59.6 ± 16.4 |
| 男性 - 例数 (%) | 71 (72.4) | 70 (79.5) |
| 体质指数 a,m±sd | 27.3 ± 6.3 | 26.5 ± 6.1 |
| 病史 | ||
| 高血压 - 例数 (%) | 31 (31.6) | 16 (18.2) |
| 糖尿病 - 例数 (%) | 10 (10.2) | 8 (9.1) |
| 心力衰竭 - 例数 (%) | 17 (17.3) | 8 (9.1) |
| 入院主要诊断 — 例数 (%) | ||
| 脓毒症 | 13 (13.3) | 10 (11.4) |
| 神经功能缺损 | 10 (10.2) | 2 (2.3) |
| 血流动力学衰竭 | 20 (20.4) | 21 (23.9) |
| 创伤 | 19 (19.4) | 16 (18.2) |
| 急性呼吸衰竭 | 22 (22.4) | 13 (14.8) |
| 急性肾损伤 | 0 (0) | 1 (1.1) |
| 失血性休克 | 3 (3.1) | 4 (4.5) |
| 代谢障碍 | 0 (0) | 2 (2.3) |
| 烧伤 | 3 (3.1) | 0 (0) |
| 术后 | 7 (7.1) | 16 (18.2) |
| 其他 | 1 (1) | 3 (3.4) |
| 入住 ICU 的原因 - 例数 (%) | ||
| 内科 | 42 (42.9) | 32 (36.4) |
| 急诊手术 | 37 (37.8) | 29 (33) |
| 择期手术 | 19 (19.4) | 27 (30.7) |
| 入选前通气持续天数,中位数 (IQR) | 14(9–18) | 11 (7.5–18.5) |
| 入组时 SOFA 评分,m±sd | 7.8 ± 3.7 | 7.1 ± 4.1 |
| SAPS II,m±sd | 45.9 ± 17.7 | 44.2 ± 16.6 |
| 入组时需要儿茶酚胺类药物的患者 - 例数 (%) | 58 (59.2) | 48 (54.5) |
| 入选时 PaO2/FiO2 比值,中位数 (IQR)b | 227 (130–340) | 250 (158–377) |
- ICU,重症监护室;m,中位数;SAPS II,简化急性生理学评分 II;sd,标准差;SOFA,序贯器官衰竭评估 0
- a “15 天” 组 91 名患者和 “8 天” 组 86 名患者的数据可用
- b 可用数据:“15 天” 组 n = 87,“8 天” 组 n = 79
# 干预
15 天组患者接受抗生素治疗的中位时间为 15 天(IQR:14-16 天),8 天组为 8 天(IQR:8-8.5 天)。延长计划的抗生素治疗时间(15 天组为 12 天,8 天组为 16 天)的主要原因是 PA-VAP 持续存在(定义为治疗结束 (EOT) 和 EOT 后 72 天之间获得的下呼吸道(LRT)培养物中存在原始基线致病原),导致延长了抗生素治疗,15 天组有 5 例,8 天组有 7 例(见补充表 1)。130 例 (71%) 患者的经验性治疗是抗生素联合治疗。118 例 (64.5%) 患者使用氨基糖苷类。经验性和确定性抗菌治疗的详细信息见附录 a。 表 2.
# 主要和次要结局
在 ITT 人群中,15 天组 25 例 (25.5%) 患者和 8 天组 31 例 (35.2%) 患者在 90 天时在 ICU 发生 PA-VAP 复发或死亡(表 2、图 2). 考虑到差异的 90% CI 上限大于 10%,未证实 8 天组相对于 15 天组的非劣效性(差异 9.7%,90% CI−1.9 至 21.2%),与在 PP 人群中进行的分析相似(n = 152,差异 12.8%,90% CI 0.4–25.6%)。考虑到基线时两组之间在心力衰竭、高血压、儿茶酚胺给药和 PaO2/FiO2 比值方面的临床相关差异,实施了一项对这些变量进行调整的事后分析,将中心作为随机效应。证实了既往结果,ITT 人群中校正的差异为 12.5%(90% CI 1.3–23.6%),与 PP 人群中进行的分析 16.3%(90% CI 3.9–28.8%) 相似。15 天组和 8 天组的 90 天总生存率相当(分别为 81.4%,90% CI 73.8–87% 和 75.6%,90% CI 66.9–82.3%,HR = 1.37,90% CI 0.81–2.33)(Supp. 图 1)。与 15 天组相比,8 天组在 ICU 住院期间 PA-VAP 复发的比例更高(几乎 2 倍)(17% vs 9.2%,差异 7.9%,90% CI−0.5–16.8%)。Fine 和 Gray 模型显示,8 天组的 PA-VAP 复发风险高于 15 天组 (sHR 1.99,CI 90%1.01-3.95)(Supp. 图 2)。
表 2 主要结局及其组成,根据研究组
| 结局或事件 | 15 天组 (N = 98) | 8 天组 (N = 88) | 差异 (90% CI) |
|---|---|---|---|
| ITT 人群中 ICU 住院期间第 90 天的死亡或 PA-VAP 复发率 - 例数 (%) | 25/98(25.5) | 31/88 (35.2) | 9.7% (− 1.9–21.2%) |
| PP 人群在 ICU 住院期间第 90 天的死亡或 PA-VAP 复发率 - 例数 (%) | 22/80(27.5) | 29/72 (40.3) | 12.8% (− 0.4–25.6%) |
| ITT 人群中 ICU 住院期间 PA-VAP 复发率 - 例数 (%) | 9/98(9.2) | 15/88 (17) | 7.9% (− 0.5–16.8%) |
- PA-VAP,铜绿假单胞菌呼吸机相关性肺炎;ICU,重症监护室;PP,符合方案;ITT,意向治疗
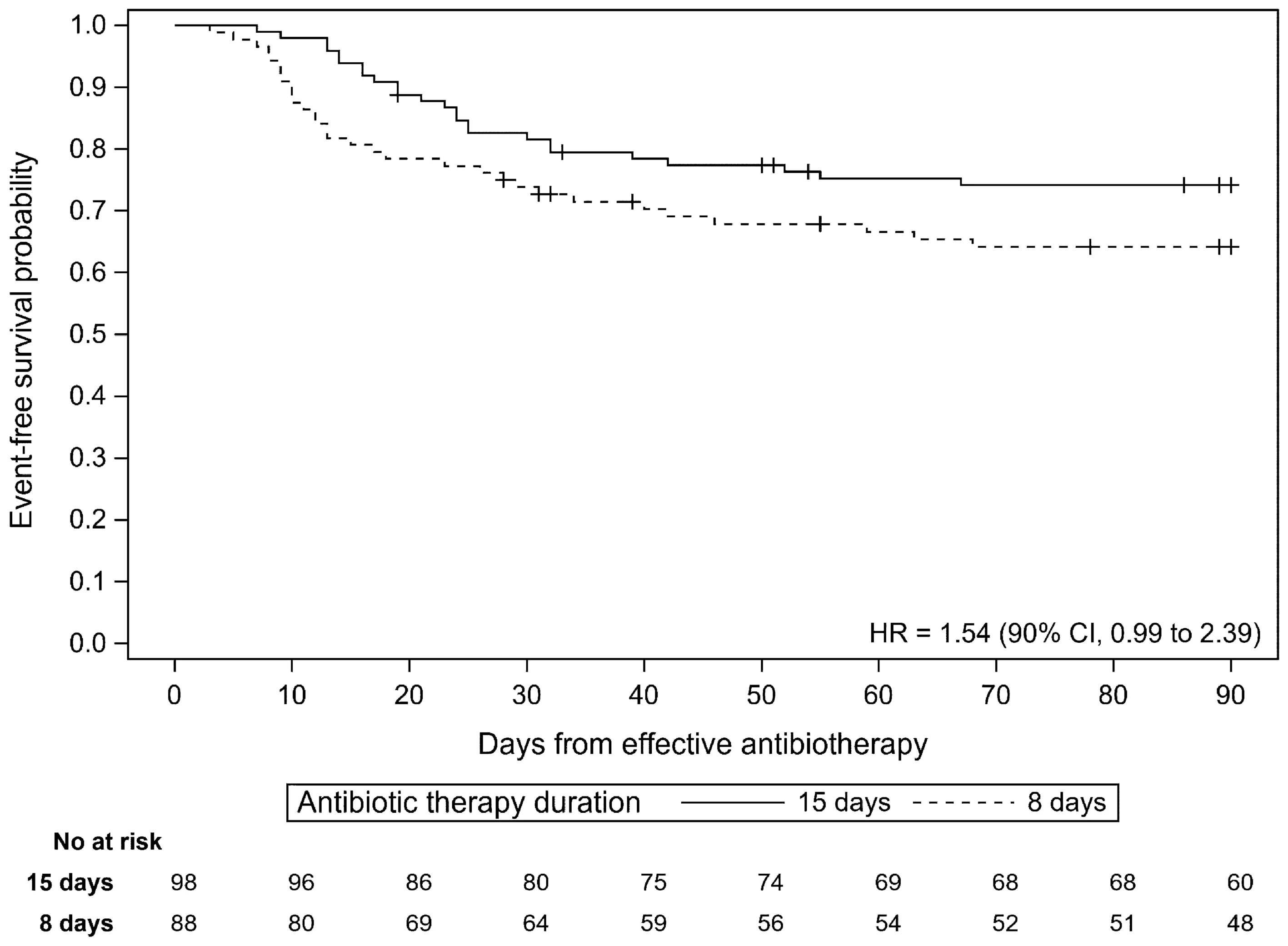
图 2 ITT 人群中 VAP 复发或 ICU 死亡生存概率的无事件生存曲线(Kaplan–Meier 估计值)。作为抗生素疗程的函数,生存概率为自开始有效抗生素治疗后 90 天
15 天组和 8 天组的机械通气持续时间 (25 (15.5–35) vs 22 (12–41))、ICU 住院时间 (34 (23–56) vs 34 (20–54))、肺外感染数量 (1 (0–2) vs 1 (0–2)) 的中位数相似,ICU 住院期间获得 MDR 病原体的比例相似 (24.7 vs 20.2%)(表 3)。与预期相同,15 天组的抗生素中位暴露量高于 8 天组,分别为 23 天(15-34 天)和 18 天(11.5-28.5 天),差异−5%(95% CI−9 至 0%)。
表 3 次要结局,根据研究组
| 结局或事件 | 15 天组 (N = 98) | 8 天组 (N = 88) | 差异 (95% CI) |
|---|---|---|---|
| 机械通气持续时间,天 a | 25 (15.5–35) | 22 (12–41) | − 3 (− 9 to 5) |
| ICU 住院时间,天 | 34 (23–56) | 34 (20–54) | 0 (− 7 to 6) |
| ICU 住院期间抗生素暴露,天 | 23 (15–34) | 18 (11.5–28.5) | − 5 (− 9 to 0) |
| ICU 住院期间的额外肺部感染次数 | 1(0–2) | 1 (0–2) | 0 (− 1 to 1) |
| 在 ICU 住院期间获得 MDR 病原体 - 例数 (%) | 24/97(24.7) | 17/84 (20.2) | − 4.5% (− 16.8 to 8.3%) |
- 数据为数量 (%) 或中位数 (IQR)
- ICU,重症监护病房;MDR,多重耐药
- a 可用数据:“15 天” 组 n = 96,“8 天” 组 n = 84
# 讨论
在这项前瞻性随机对照试验中,在成人 PA-VAP 患者中,未证实短期策略(8 天)相比长期策略(15 天)在 90 天内 ICU 住院期间发生的死亡率和 PA-VAP 复发复合终点方面的非劣效性。此外,8 天组 PA-VAP 复发的可能性是 15 天组的 2 倍。此外,考虑到 8 天组与 15 天组的竞争性死亡风险,Fine 和 Gray 模型显示 PA-VAP 复发风险更高。虽然 8 天组患者在 ICU 住院期间抗生素暴露确实较少,但我们在 15 天组中未发现更多的多重耐药病原体。
虽然治疗 VAP 的抗生素疗程仍是一个挑战,但只有少数随机对照试验解决了这个问题。两项研究比较了 8 vs. 15 天抗生素疗程 [[5]、[13]],另外两项研究比较了 7 天与 10 天 [[14]、[15],一项研究比较了 8 天与 12 天 [[16]]。2 篇已发表的系统综述发现短期和长期抗生素治疗在 28 天死亡率 [6]、机械通气持续时间或 ICU 住院时间 [6]、[17] 方面无差异。然而,在非发酵革兰阴性菌的患者子集中,长期组的复发率有降低趋势。Capellier 等 [[13]] 对早发性 VAP 的研究中,8d 组继发感染率高于 15d 组。在 PneumA 研究中,NF-GNB 治疗 8 天引起的 VAP 患者有更高的复发感染率(40.6% 与 25.4%)。最后,274 例迟发性 VAP 患者中,一项随机对照试验表明,7 天疗程的临床失败率和 28 天死亡率并不显著高于固定的 10 天疗程 [[15]。在我们的试验中,7 天组(ITT 人群)PA-VAP 死亡或复发的患者百分比为 35.2%,接近 Planquette 等观察到的 35.7% 的 PA-VAP 死亡率和 / 或复发率。在一项 393 名 PA-VAP [11] 患者的回顾性研究中,存活者的中位抗生素使用时间为 9 天 (IQR,6–12)。
尽管复发率较高,但在我们的研究中,短期策略与死亡率增加、机械通气持续时间延长或 ICU 住院时间延长无关。因此,在得出抗生素治疗非发酵 GNB 所致 VAP 的最佳疗程的任何明确结论之前,似乎还需要更多的研究。不能排除为期 8 天的治疗,但我们的结果请根据密切的临床和生物学监测采取审慎的方法,尽管在我们的研究中未对此进行检测。可对生物标志物进行评估,以专门监测这种情况下的疗程。
据我们所知,本研究是首个专门针对 PA-VAP 的随机对照试验。在我们的试验中,主要结局组成成分的预期发生率被正确估计:15 天组 PA-VAP 死亡或复发的患者百分比为 27.5%,8 天组为 40.3%。这些比例与现有研究的结果一致 [17]。完全遵守方案计划的抗生素疗程,15 天和 8 天组的中位疗程分别是 15 天和 8 天,这与预期一致。抗生素治疗计划持续时间的依从性可接受(约 80%)(见增补表 2)。
主要的局限性是,尽管整个法国的 30 家中心(包括大学和非大学医院的内科、外科和普通重症监护室)参与了研究,但研究最终仅纳入了最初计划的 33% 的患者。事实上,由于在 ICU 住院期间 PA-VAP 发作较晚,许多患者已纳入其他干预性研究中,因此我们的试验未纳入这些患者。事后敏感性 Bayesian 分析表明,ITT 人群中的非劣效性概率接近 55%,PP 人群中接近 40%(补充文件 2)。
总之,由于复发率较高,我们的试验没有证明抗生素治疗 8 天相对于 15 天的非劣效性。我们的结果的不确定性可能与统计学效度不足有关。
# References
Kalil AC, Metersky ML, Klompas M et al (2016) Management of adults with hospital-acquired and ventilator-associated pneumonia: 2016 clinical practice guidelines by the Infectious Diseases Society of America and the American Thoracic Society. Clin Infect Dis 63(5):e61–e111. [https://doi.org/10.1093/cid/ciw353]
Torres A, Niederman MS, Chastre J et al (2017) International ERS/ESICM/ESCMID/ALAT guidelines for the management of hospital-acquired pneumonia and ventilator-associated pneumonia: Guidelines for the management of hospital-acquired pneumonia (HAP)/ventilator-associated pneumonia (VAP) of the European Respiratory Society (ERS), European Society of Intensive Care Medicine (ESICM), European Society of Clinical Microbiology and Infectious Diseases (ESCMID) and Asociación Latinoamericana del Tórax (ALAT). Eur Respir J. [https://doi.org/10.1183/13993003.00582-2017]
Leone M, Bouadma L, Bouhemad B et al (2018) Hospital-acquired pneumonia in ICU. Anaesth Crit Care Pain Med 37(1):83–98. [https://doi.org/10.1016/j.accpm.2017.11.006]
Hurley JC (2019) Worldwide variation in Pseudomonas associated ventilator associated pneumonia. A meta-regression. J Crit Care 51:88–93. [https://doi.org/10.1016/j.jcrc.2019.02.001]
Chastre J, Wolff M, Fagon JY et al (2003) Comparison of 8 vs 15 days of antibiotic therapy for ventilator-associated pneumonia in adults: a randomized trial. JAMA 290(19):2588. [https://doi.org/10.1001/jama.290.19.2588]
Pugh R, Grant C, Cooke RPD, Dempsey G (2015) Short-course versus prolonged-course antibiotic therapy for hospital-acquired pneumonia in critically ill adults. Cochrane Database Syst Rev 8:CD007577. [https://doi.org/10.1002/14651858.CD007577.pub3]
Combes A, Luyt CE, Fagon JY, Wolff M, Trouillet JL, Chastre J (2007) Early predictors for infection recurrence and death in patients with ventilator-associated pneumonia. Crit Care Med 35(1):146–154. [https://doi.org/10.1097/01.CCM.0000249826.81273.E4]
Bouglé A, Foucrier A, Dupont H et al (2017) Impact of the duration of antibiotics on clinical events in patients with Pseudomonas aeruginosa ventilator-associated pneumonia: study protocol for a randomized controlled study. Trials 18(1):37. [https://doi.org/10.1186/s13063-017-1780-3]
Toulouse E, Lafont B, Granier S, Mcgurk G, Bazin JE (2020) French legal approach to patient consent in clinical research. Anaesth Crit Care Pain Med 39(6):883–885. [https://doi.org/10.1016/j.accpm.2020.10.012]
European Medicines Agency (2013) Addendum to the guideline on the evaluation of medicinal products indicated for treatment of bacterial infections. Committee for Human Medicinal Products
Planquette B, Timsit JF, Misset BY et al (2013) Pseudomonas aeruginosa ventilator-associated pneumonia. Predictive factors of treatment failure. Am J Respir Crit Care Med 188(1):69–76. [https://doi.org/10.1164/rccm.201210-1897OC]
Berry DA (1996) Statistics: a Bayesian perspective
Capellier G, Mockly H, Charpentier C et al (2012) Early-onset ventilator-associated pneumonia in adults randomized clinical trial: comparison of 8 versus 15 days of antibiotic treatment. PLoS ONE 7(8):e41290. [https://doi.org/10.1371/journal.pone.0041290]
Fekih Hassen M, Ayed S, Ben Sik Ali H, Gharbi R, Marghli S, Elatrous S (2009) Duration of antibiotic therapy for ventilator-associated pneumonia: comparison of 7 and 10 days. A pilot study. Ann Fr Anesth Reanim 28(1):16–23. [https://doi.org/10.1016/j.annfar.2008.10.021]
Kollef MH, Chastre J, Clavel M et al (2012) A randomized trial of 7-day doripenem versus 10-day imipenem-cilastatin for ventilator-associated pneumonia. Crit Care 16(6):R218. [https://doi.org/10.1186/cc11862]
Medina J, Perez Protto S, Paciel D, Pontet J, Saldun P, Berro M (2007) Antibiotic treatment for the ventilator-associated pneumonia: 8 vs 12 days randomized trial preliminary data. In: Proceedings of the 47th interscience conference on antimicrobial agents and chemotherapy, Chicago, IL, 17–20 Sept 2007, p 361
Dimopoulos G, Poulakou G, Pneumatikos IA, Armaganidis A, Kollef MH, Matthaiou DK (2013) Short- vs long-duration antibiotic regimens for ventilator-associated pneumonia: a systematic review and meta-analysis. Chest 144(6):1759–1767. [https://doi.org/10.1378/chest.13-0076]
